Hvad sker der, når sølv tilsættes til kobbersulfatopløsning?
* sølv er mere reaktiv end kobber. Dette betyder, at sølv har en stærkere tendens til at miste elektroner og danne positive ioner (AG⁺).
* Kobberioner (cu²⁺) i opløsningen tiltrækkes af sølvet. Sølvatomerne donerer elektroner til kobberionerne, hvilket får dem til at reducere til kobberatomer (Cu).
* sølvioner (AG⁺) dannes. De sølvatomer, der donerer elektroner, bliver sølvioner.
* Løsningen ændrer farve. Den blå farve på kobbersulfatopløsningen falmer, når kobberioner fjernes, og opløsningen kan blive lidt overskyet, når kobbermetal udfælder.
Her er den kemiske ligning:
2AG (S) + CUSO₄ (AQ) → CU (S) + AG₂SO₄ (AQ)
i enklere termer:
* Sølv (AG) fortrænger kobber (Cu) fra kobbersulfatopløsningen.
* Sølv danner sølvsulfat (ag₂so₄), der opløses i opløsningen.
* Kobbermetal (Cu) udfælder ud af opløsningen som et rødbrunt fast stof.
Nøgleobservationer:
* Dannelse af et rødbrunt fast stof (kobbermetal)
* Fading af den blå farve på kobbersulfatopløsningen
* mulig let uklarhed i løsningen
 Varme artikler
Varme artikler
-
 Lysbaseret produktion af lægemiddel-opdagelsesmolekylerKredit:CC0 Public Domain Fotoelektrokemiske (PEC) celler er bredt undersøgt for omdannelse af solenergi til kemiske brændstoffer. De bruger fotokatoder og fotoanoder til at spalte vand til henhold
Lysbaseret produktion af lægemiddel-opdagelsesmolekylerKredit:CC0 Public Domain Fotoelektrokemiske (PEC) celler er bredt undersøgt for omdannelse af solenergi til kemiske brændstoffer. De bruger fotokatoder og fotoanoder til at spalte vand til henhold -
 Regelfølgende molekyler giver den første direkte bekræftelse af en halvt århundrede gammel teoriFig. S1. AIMS Wavepacket Population for aksiale og ækvatoriale konformere. (Top) Woodward-Hoffman tillod fotoprodukter fra økse og eq αPH (isopropylgruppen er repræsenteret som R-gruppen). (Nederst) B
Regelfølgende molekyler giver den første direkte bekræftelse af en halvt århundrede gammel teoriFig. S1. AIMS Wavepacket Population for aksiale og ækvatoriale konformere. (Top) Woodward-Hoffman tillod fotoprodukter fra økse og eq αPH (isopropylgruppen er repræsenteret som R-gruppen). (Nederst) B -
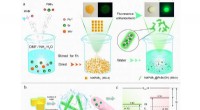 Blyhalogenid perovskiter med forbedret luminescens og stabiliteta) Skematisk diagram af synteseprocessen for MAPbBr3@PbBr(OH). b) Skematisk illustration af morfologiudviklingen af den fremstillede MAPbBr3-perovskit. c) Energiniveaudiagram af PbBr(OH) og indre QD
Blyhalogenid perovskiter med forbedret luminescens og stabiliteta) Skematisk diagram af synteseprocessen for MAPbBr3@PbBr(OH). b) Skematisk illustration af morfologiudviklingen af den fremstillede MAPbBr3-perovskit. c) Energiniveaudiagram af PbBr(OH) og indre QD -
 Metalion-gennembrud fører til nye biomaterialerMetaller som jern og calcium spiller en afgørende rolle i den menneskelige krop, så det er ingen overraskelse, at bioingeniører gerne vil integrere dem i det bløde, strækbare materialer, der bruges ti
Metalion-gennembrud fører til nye biomaterialerMetaller som jern og calcium spiller en afgørende rolle i den menneskelige krop, så det er ingen overraskelse, at bioingeniører gerne vil integrere dem i det bløde, strækbare materialer, der bruges ti
- Eksperter bevæger sig et skridt tættere på at afmystificere kvanteverdenen
- To-foton mikroskopi:Ny forskning kan bidrage drastisk til at reducere omkostningerne ved kraftfuld m…
- Citizen science-programmer giver værdifulde data om intermitterende floder i det sydvestlige USA
- Peloton sælger sine cykler på Amazon for at vende nedturen
- Hvordan holdes kovalente bindinger sammen?
- Hvilke stoffer produceres i fotosyntese og respiration?


