Hvorfor er reaktionen SO2 plus H2O H2SO2 ikke afbalanceret?
reaktanter:
* s: 1 atom
* o: 3 atomer (2 fra SO2 og 1 fra H2O)
* h: 2 atomer
Produkter:
* s: 1 atom
* o: 2 atomer
* h: 2 atomer
Problemet: Der er 3 iltatomer på reaktantsiden og kun 2 på produktsiden.
For at afbalancere ligningen skal du justere koefficienterne foran de kemiske formler:
SO2 + H2O -> H2SO3
Forklaring af den afbalancerede ligning:
* SO2: 1 molekyle (1 svovlatom og 2 iltatomer)
* H2O: 1 molekyle (2 hydrogenatomer og 1 iltatom)
* H2SO3: 1 molekyle (2 hydrogenatomer, 1 svovlatom og 3 iltatomer)
Nu er ligningen afbalanceret:
* s: 1 atom på hver side
* o: 3 atomer på hver side
* h: 2 atomer på hver side
Vigtig note: Produktet af reaktionen er faktisk svovlsyre (H2SO3) , ikke H2SO2 .
 Varme artikler
Varme artikler
-
 Forskere gengiver maleri i stor skala Great Wave med inkless teknologiRadical Inkless Technology producerer verdens mindste Ukiyo-e og lover at revolutionere vores udskrivning. Kredit:Kyoto University iCeMS Katsushika Hokusai (1760 - 1849) er titanen for japansk kun
Forskere gengiver maleri i stor skala Great Wave med inkless teknologiRadical Inkless Technology producerer verdens mindste Ukiyo-e og lover at revolutionere vores udskrivning. Kredit:Kyoto University iCeMS Katsushika Hokusai (1760 - 1849) er titanen for japansk kun -
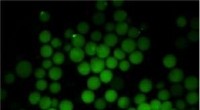 Små geler opsuger intestinale toksinerMikrogeler er vist ovenfor med sukkermotiver efter binding fluorescensmærkede lektiner. Kredit:Alexander Kuehne Bakterielle infektioner, der er målrettet mod tarmen, kan forårsage tilstande, der s
Små geler opsuger intestinale toksinerMikrogeler er vist ovenfor med sukkermotiver efter binding fluorescensmærkede lektiner. Kredit:Alexander Kuehne Bakterielle infektioner, der er målrettet mod tarmen, kan forårsage tilstande, der s -
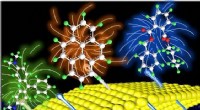 Ny Raman-metode fanger målmolekyler i små huller aktivtSkematisk diagram af princippet om den generelle overfladeforstærkede Raman-spektroskopimetode til aktivt at fange målmolekyler i små huller med opløsningsmidlet. Kredit:GE Meihong For nylig, Prof
Ny Raman-metode fanger målmolekyler i små huller aktivtSkematisk diagram af princippet om den generelle overfladeforstærkede Raman-spektroskopimetode til aktivt at fange målmolekyler i små huller med opløsningsmidlet. Kredit:GE Meihong For nylig, Prof -
 Ny elektroorganisk syntese muliggør bæredygtig og grøn produktion af finkemikalierEn forsker, der opretter et flowelektrolyseeksperiment. Kredit:©:Alexander Sell, JGU I det kooperative forskningsprojekt EPSYLON finansieret af det tyske forbundsministerium for uddannelse og fors
Ny elektroorganisk syntese muliggør bæredygtig og grøn produktion af finkemikalierEn forsker, der opretter et flowelektrolyseeksperiment. Kredit:©:Alexander Sell, JGU I det kooperative forskningsprojekt EPSYLON finansieret af det tyske forbundsministerium for uddannelse og fors
- Anvendelse af fordelsdestillation til enhedsuafhængig kvantenøgledistribution (DIQKD)
- Nikkel adskillelse, rumlig kationfordeling og tæt integrerede faser forekommer i uberørt batterima…
- Skydråbernes hemmelige liv
- Hvad er 362 031 100 km2 videnskabelig notation?
- Grundstof 3 lithium har en valenselektron og grundstof 4 beryllium to elektroner 5 bor hvor mange el…
- Hvad er det kemiske navn på eksotermisk?


