Hvorfor bruges fast NAHCO3 i stedet for vandigt i syntese-tert-butylchloridet?
* reaktionsmekanisme: Syntesen af T-Bucl involverer normalt reaktionen af tert-butanol (T-BuOH) med saltsyre (HCI). Reaktionen producerer vand som et biprodukt:
T-BUOH + HCL → T-BUCL + H₂O
* bivirkninger: Vand er en god nukleofil, og i nærvær af HCI kan det konkurrere med T-BuOH om det elektrofile chloridion (CL⁻). Dette fører til dannelse af uønskede biprodukter.
* vandigt natriumbicarbonats rolle: Vandigt natriumbicarbonat fungerer som en base For at neutralisere HCI og fjerne vand fra reaktionsblandingen. Bicarbonationerne (HCO₃⁻) reagerer med H⁺ioner for at danne kulsyre (H₂CO₃), som hurtigt nedbrydes i kuldioxid (CO₂) og vand:
HCO₃⁻ + H⁺ → H₂CO₃ → CO₂ + H₂O
Dette driver ligevægten mod dannelsen af T-BUCL, når vandet fjernes.
Kortfattet:
* fast natriumbicarbonat: Det bruges ikke til syntese af T-BUCL, fordi den ikke let er opløselig i reaktionsblandingen, og dens faste form ville ikke være effektiv til at neutralisere HCI og fjerne vand.
* vandigt natriumbicarbonat: Det bruges, fordi det giver en kilde til bicarbonationer til at neutralisere HCI, fjerne vand og fremme den ønskede reaktion.
Fortæl mig, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
 Hærforskere opdager magt i urinenMenneskelig urin er omkring 96 procent vand og fire procent affaldsstoffer, men der er mere end 3, 000 forbindelser findes i væsken. Hærforskere eksperimenterer med at producere brint fra urin. Kredit
Hærforskere opdager magt i urinenMenneskelig urin er omkring 96 procent vand og fire procent affaldsstoffer, men der er mere end 3, 000 forbindelser findes i væsken. Hærforskere eksperimenterer med at producere brint fra urin. Kredit -
 Går småt for at bestemme, hvor nukleart materiale kom fra, og hvordan det blev lavetIn-situ uran-isotop-billeddannelse af NanoSIMS kan give indsigt i proceshistorien og oprindelsen af materialer til nukleare brændstofpellets til støtte for nuklear retsmedicinske undersøgelser. Kred
Går småt for at bestemme, hvor nukleart materiale kom fra, og hvordan det blev lavetIn-situ uran-isotop-billeddannelse af NanoSIMS kan give indsigt i proceshistorien og oprindelsen af materialer til nukleare brændstofpellets til støtte for nuklear retsmedicinske undersøgelser. Kred -
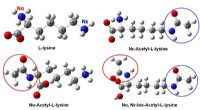 Raman og infrarød spektroskopi hjælper med at identificere forskellige acetylerede lysinerMolekylære strukturer af lysin og tre acetylerede lysiner. Kredit:Yao Guohua Et forskerhold ledet af prof. Huang Qing fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabs
Raman og infrarød spektroskopi hjælper med at identificere forskellige acetylerede lysinerMolekylære strukturer af lysin og tre acetylerede lysiner. Kredit:Yao Guohua Et forskerhold ledet af prof. Huang Qing fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabs -
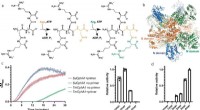 De overraskende schweizerkniv-lignende funktioner af et kraftfuldt enzymCphA1 struktur og aktivitet. a Skematisk diagram af de biosyntetiske reaktioner katalyseret af G- og M-domænerne af CphA1. b Den overordnede struktur af tetramer CphA1 fra Synechocystis sp. UTEX2470 (
De overraskende schweizerkniv-lignende funktioner af et kraftfuldt enzymCphA1 struktur og aktivitet. a Skematisk diagram af de biosyntetiske reaktioner katalyseret af G- og M-domænerne af CphA1. b Den overordnede struktur af tetramer CphA1 fra Synechocystis sp. UTEX2470 (
- Hvorfor bruger videnskabsmand Robert Hazen trykbomber til at sprænge mineraler?
- To af verdens tearter uddøde i naturen ifølge ny rapport
- Hvilken form for teknologi er videnskabsmand, der mest sandsynligt bruger, beregne afstanden til en …
- Ny forskning i spredning af infektioner afslører behov for større samarbejde mellem biologi og fys…
- Sådan beregnes frysepunktet for en blanding
- Hydrogelglas:et nyt glasdesign til energibesparelser i bygninger


