Hvordan beregner du, hvor mange gram vand der produceres fra 22,1 ilt?
1. Skriv den afbalancerede kemiske ligning:
Reaktionen til dannelse af vand er:
2H₂ + O₂ → 2H₂O
Dette betyder 2 mol brint (H₂) reagerer med 1 mol ilt (O₂) for at producere 2 mol vand (H₂O).
2. Beregn mol ilt:
* Find den molære masse af ilt (O₂):16 g/mol (O) * 2 =32 g/mol (O₂)
* Opdel massen af ilt med dens molære masse:22,1 g / 32 g / mol =0,691 mol O₂
3. Bestem mol produceret vand:
* Brug molforholdet fra den afbalancerede ligning:1 mol O₂ producerer 2 mol H₂O
* Multiplicer molen af ilt med molforholdet:0,691 mol O₂ * (2 mol H₂O / 1 mol O₂) =1,382 mol H₂O
4. Beregn gram vand:
* Find den molære masse af vand (H₂O):1 g/mol (H) * 2 + 16 g/mol (O) =18 g/mol (H₂O)
* Multiplicer molen af vand med dets molære masse:1,382 mol H₂O * 18 g/mol =24,88 g H₂O
Derfor produceres ca. 24,88 gram vand fra 22,1 gram ilt.
 Varme artikler
Varme artikler
-
 Organisk kationinterkalering:En effektiv strategi til manipulation af båndtopologi og superledningKredit:CC0 Public Domain I en nylig artikel offentliggjort i Videnskabsbulletin , forskere udviklede en effektiv organisk-kation-interkalationsstrategi til at manipulere mellemlagskoblingen af
Organisk kationinterkalering:En effektiv strategi til manipulation af båndtopologi og superledningKredit:CC0 Public Domain I en nylig artikel offentliggjort i Videnskabsbulletin , forskere udviklede en effektiv organisk-kation-interkalationsstrategi til at manipulere mellemlagskoblingen af -
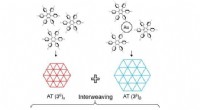 Meget kompleks todimensionel tessellation i den molekylære verdenFigur viser tre typer af meget komplekse sammenvævede tesselleringer baseret på to forskellige molekylære faser konstrueret af en enkelt molekylær byggesten. Kredit:Nature Communications Tessellat
Meget kompleks todimensionel tessellation i den molekylære verdenFigur viser tre typer af meget komplekse sammenvævede tesselleringer baseret på to forskellige molekylære faser konstrueret af en enkelt molekylær byggesten. Kredit:Nature Communications Tessellat -
 Knækning af colibactins kode:Undersøgelse undersøger, hvordan sammensatte beskadigede DNA for at …Escherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH I mere end et årti, forskere har arbejdet på at forstå sammenhængen mellem colibactin, en forbindelse fremstillet af visse stammer
Knækning af colibactins kode:Undersøgelse undersøger, hvordan sammensatte beskadigede DNA for at …Escherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH I mere end et årti, forskere har arbejdet på at forstå sammenhængen mellem colibactin, en forbindelse fremstillet af visse stammer -
 Sneglelim afslører ledetråde til at lave bedre medicinske klæbemidlerForskere studerer, hvordan sneglelim opnår sin stærke klæbeevne og fleksibilitet, indsigt, der kunne bruges til at skabe bedre medicinske klæbemidler. Kredit:Rebecca Falconer, Ithaca College Dusky
Sneglelim afslører ledetråde til at lave bedre medicinske klæbemidlerForskere studerer, hvordan sneglelim opnår sin stærke klæbeevne og fleksibilitet, indsigt, der kunne bruges til at skabe bedre medicinske klæbemidler. Kredit:Rebecca Falconer, Ithaca College Dusky
- Forskere knækker strukturen af nøgleprotein i Zika-virus
- Hvad sker der, når cellerne formerer sig uden kontrol?
- Hvad er en faldet stjerne?
- Billede:Koldt plasma testet på ISS
- Eksperten diskuterer strømforbruget for næste generations trådløse netværk
- Meteoritter:Hvorfor studere dem? Hvad kan de lære os om at finde liv hinsides Jorden?


