Hvad er mere flygtigt benzen eller toluen?
volatilitet henviser til et stofs tendens til at fordampe eller fordampe. Jo højere volatilitet, jo lettere er det for et stof at omdanne fra en væske til en gas.
Faktorer, der påvirker volatiliteten:
* Intermolekylære kræfter: Svagere intermolekylære kræfter resulterer i højere volatilitet.
* molekylvægt: Forbindelser med lavere molekylvægt har en tendens til at være mere flygtige.
* damptryk: Højere damptryk indikerer større volatilitet.
Sammenligning af benzen og toluen:
* molekylvægt: Toluen (92,14 g/mol) har en lidt højere molekylvægt end benzen (78,11 g/mol).
* Intermolekylære kræfter: Både benzen og toluen er ikke -polære molekyler, der primært holdes sammen af London -spredningskræfter. Toluen har imidlertid et større overfladeareal og større polariserbarhed, hvilket fører til lidt stærkere London -spredningskræfter.
* damptryk: Toluen har et højere damptryk end benzen ved en given temperatur.
Konklusion:
Selvom forskellen i volatilitet mellem benzen og toluen er relativt lille, betragtes toluen som mere flygtig på grund af dets højere damptryk og lidt svagere intermolekylære kræfter.
Sidste artikelHvad er produktet af natrium og brint?
Næste artikelFormer klor en positiv eller negativ ion?
 Varme artikler
Varme artikler
-
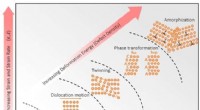 Øer uden struktur inde i metallegeringer kan føre til hårdere materialerForeslået hierarkisk deformationsmekanisme-paradigme for de ækviatomiske CrCoNi-baserede HEAer udsat for stigende grader af deformation. Elastisk deformation, dislokationsmedieret plasticitet, twinnin
Øer uden struktur inde i metallegeringer kan føre til hårdere materialerForeslået hierarkisk deformationsmekanisme-paradigme for de ækviatomiske CrCoNi-baserede HEAer udsat for stigende grader af deformation. Elastisk deformation, dislokationsmedieret plasticitet, twinnin -
 Det, vi vidste om vand, var trods alt rigtigtDannelsen af hydrogenperoxid ved luft-vand-grænsefladen i mikrodråber er ikke spontan som tidligere antaget, men er i stedet drevet af ozon. Kredit:KAUST En omfattende undersøgelse foretaget af K
Det, vi vidste om vand, var trods alt rigtigtDannelsen af hydrogenperoxid ved luft-vand-grænsefladen i mikrodråber er ikke spontan som tidligere antaget, men er i stedet drevet af ozon. Kredit:KAUST En omfattende undersøgelse foretaget af K -
 Ny metode til mikrobiel energiproduktion opdagetPaul King, David Mulder og Cara Lubner, medforfattere af papiret “Mechanistic Insights into Energy Conservation by Flavin-Based Electron Bifurcation, ”Stå ved siden af en laser kombineret med et spe
Ny metode til mikrobiel energiproduktion opdagetPaul King, David Mulder og Cara Lubner, medforfattere af papiret “Mechanistic Insights into Energy Conservation by Flavin-Based Electron Bifurcation, ”Stå ved siden af en laser kombineret med et spe -
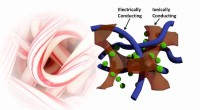 Candy cane polymer vævning kan drive fremtidige funktionelle stoffer og enhederSuperkondensatorer vævet som den røde og hvide af en slikstok kunne have øget opbevaringskapacitet i forhold til den nuværende teknologi. Kredit:Tiesheng Wang Hvis forskere nogensinde vil leve op
Candy cane polymer vævning kan drive fremtidige funktionelle stoffer og enhederSuperkondensatorer vævet som den røde og hvide af en slikstok kunne have øget opbevaringskapacitet i forhold til den nuværende teknologi. Kredit:Tiesheng Wang Hvis forskere nogensinde vil leve op
- Marine bakterielt exopolysaccharid EPS11 hæmmer migration og invasion af levercancerceller
- Hvad er forskellen mellem en syre og en base noget, der neutral?
- Hvilken planet var den første, der blev besøgt af rumfartøjet?
- Hvad tror de fleste forskere er oprindelsen af måner?
- Hvorfor er frugten orange i videnskaben?
- 10 måder at stoppe en morder -asteroide


