Hvorfor skulle CL få elektronet?
* Elektronegativitet: Klor er mere elektronegativ end natrium. Elektronegativitet er et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding. Klor har en højere elektronegativitet end natrium, hvilket betyder, at det har et stærkere træk på elektroner.
* octet regel: Både natrium og klor ønsker at opnå en stabil elektronkonfiguration som en ædel gas. Natrium har en valenselektron i sin yderste skal, mens klor har syv. Ved at få en elektron afslutter klor sin oktet (otte elektroner i sin yderste skal), hvilket gør den stabil.
* ionisk bindingsdannelse: Når natrium- og klorreaktioner, mister natrium let sin ene valenselektron for at blive en positivt ladet ion (Na+). Denne elektron opnås derefter ved klor, hvilket gør det til en negativt ladet ion (Cl-). De modsatte ladninger mellem Na+ og Cl- tiltrækker derefter hinanden, danner en ionisk binding og skaber den sammensatte NaCl.
Kortfattet: Klor får en elektron i NaCI, fordi det er mere elektronegativt, og ved at gøre det opnår det en stabil elektronkonfiguration og opfylder Octet -reglen. Denne elektronoverførsel danner en ionisk binding mellem det positivt ladede natriumion og den negativt ladede chloridion.
Sidste artikelHvorfor er vandmolekyler tiltrukket af hinanden?
Næste artikelHvilken forbindelse har 1 kaliumnitrogen og 3
 Varme artikler
Varme artikler
-
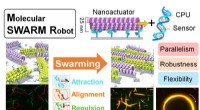 Forskere, der arbejder på at få robotter på størrelse med molekyler til at sværme sammen for at…En molekylær robot, som typisk er mellem 100 nanometer og 100 mikrometer lang, kræver en aktuator, processor og sensor for at fungere korrekt. Ved at finjustere deres gensidige interaktioner, millione
Forskere, der arbejder på at få robotter på størrelse med molekyler til at sværme sammen for at…En molekylær robot, som typisk er mellem 100 nanometer og 100 mikrometer lang, kræver en aktuator, processor og sensor for at fungere korrekt. Ved at finjustere deres gensidige interaktioner, millione -
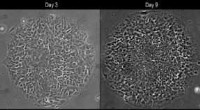 Mod en stamcellemodel for udvikling af menneskeligt nervesystemSkiveformede kolonier vist med fasekontrast (øverst) og fluorescens (nederst) mikroskopi. Mellem dag 3 og dag 9, celler i midten af kolonien vokser hurtigere og bliver meget tættere pakket. Begrænse
Mod en stamcellemodel for udvikling af menneskeligt nervesystemSkiveformede kolonier vist med fasekontrast (øverst) og fluorescens (nederst) mikroskopi. Mellem dag 3 og dag 9, celler i midten af kolonien vokser hurtigere og bliver meget tættere pakket. Begrænse -
 Påvisning af blodpletter - med en antimalarial forbindelseAt fortælle hvilken plet på disse papirfiltre (øverste række) er fra blod (C) frem for kaffe (A) eller te (B) er lettere med en ny forbindelse, der reagerer med blod og lyser i mørket (nederste række,
Påvisning af blodpletter - med en antimalarial forbindelseAt fortælle hvilken plet på disse papirfiltre (øverste række) er fra blod (C) frem for kaffe (A) eller te (B) er lettere med en ny forbindelse, der reagerer med blod og lyser i mørket (nederste række, -
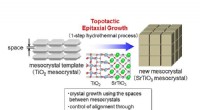 Fotokatalysator gør brintproduktion 10 gange mere effektivSyntese af SrTiOmeso-krystaller ved topotaktisk epitaksial vækst. Kredit:Kobe University Brint er en alternativ energikilde, der kan produceres fra vedvarende kilder til sollys og vand. En gruppe
Fotokatalysator gør brintproduktion 10 gange mere effektivSyntese af SrTiOmeso-krystaller ved topotaktisk epitaksial vækst. Kredit:Kobe University Brint er en alternativ energikilde, der kan produceres fra vedvarende kilder til sollys og vand. En gruppe


