Jernsulfat reagerer ikke med kobber hvorfor?
* reaktivitetsserien: Metaller er arrangeret i en reaktivitetsserie baseret på deres tendens til at miste elektroner og danne positive ioner. Metaller, der er højere i serien, er mere reaktive.
* forskydningsreaktioner: Når et mere reaktivt metal anbringes i en opløsning af et mindre reaktivt metals salt, vil det fortrænge det mindre reaktive metal fra opløsningen.
* kobber og jern: I dette tilfælde er jern højere i reaktivitetsserien end kobber. Dette betyder, at jern er mere tilbøjeligt til at miste elektroner og danne ioner end kobber.
Derfor, hvis du skulle placere et stykke kobber i en opløsning af jernsulfat, ville ingen reaktion forekomme, fordi kobber ikke kan fortrænge jern fra dets salt.
Sammendrag: Den reaktion, du beskriver, er en enkelt forskydningsreaktion, og for at den kan forekomme, skal metallet i opløsningen være mindre reaktiv end det metal, der tilsættes. Da kobber er mindre reaktiv end jern, forekommer der ingen reaktion.
Sidste artikelHvor mange kovalente bindinger dannes fluor?
Næste artikelEr brint og gas det samme?
 Varme artikler
Varme artikler
-
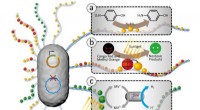 Konstruerede bakterielle biofilm, der immobiliserer nanopartikler, muliggør forskellige katalytiske…Forskellige katalytiske anvendelser af tunable funktionel E coli biofilm med forankrede nanoobjekter. (a) De biofilmforankrede Au NPer muliggør den genanvendelige katalytiske reduktion af den giftig
Konstruerede bakterielle biofilm, der immobiliserer nanopartikler, muliggør forskellige katalytiske…Forskellige katalytiske anvendelser af tunable funktionel E coli biofilm med forankrede nanoobjekter. (a) De biofilmforankrede Au NPer muliggør den genanvendelige katalytiske reduktion af den giftig -
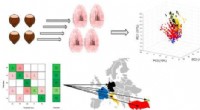 Godkendelse af hasselnøddernes geografiske oprindelseKredit:American Chemical Society Hasselnødder, som olivenolie, ost og andre landbrugsprodukter varierer i smag afhængigt af deres geografiske oprindelse. Fordi forbrugere og processorer er villige
Godkendelse af hasselnøddernes geografiske oprindelseKredit:American Chemical Society Hasselnødder, som olivenolie, ost og andre landbrugsprodukter varierer i smag afhængigt af deres geografiske oprindelse. Fordi forbrugere og processorer er villige -
 Mønstergenkendelse af kemiske bølger i Belousov-Zhabotinsky kemiske reaktionDeres projekt involverede den kemiske reaktion Belousov-Zhabotinsky-et eksempel på en kemisk oscillator, der ofte bruges til at illustrere et kaotisk system. Kredit:University of Exeter Et kollabo
Mønstergenkendelse af kemiske bølger i Belousov-Zhabotinsky kemiske reaktionDeres projekt involverede den kemiske reaktion Belousov-Zhabotinsky-et eksempel på en kemisk oscillator, der ofte bruges til at illustrere et kaotisk system. Kredit:University of Exeter Et kollabo -
 Platinfri katalysatorer kunne lave billigere brintbrændselscellerEksperimentel opsætning ved den avancerede fotonkilde, Materials Research Collaborative Access Teams beamline 10-ID til røntgenabsorptionsanalyse af elektrokatalysatorprækursorer under pyrolyse. Kredi
Platinfri katalysatorer kunne lave billigere brintbrændselscellerEksperimentel opsætning ved den avancerede fotonkilde, Materials Research Collaborative Access Teams beamline 10-ID til røntgenabsorptionsanalyse af elektrokatalysatorprækursorer under pyrolyse. Kredi
- Forskere finder beviser på, at Venus har aktive vulkaner
- Den hastighed, hvormed du rejser i rummet uden hjælp?
- En forbindelse, der indeholder et atom af kulstof for hver to atomer Oxygen har formlen er CO?
- HVEM, Greta eller pressens vagthunde til Nobels Fredspris?
- Hvordan måler forskere størrelsen af orkaner?
- Hvad er den omtrentlige energi fra en foton, der har frekvens 4x10 til 7. strøm?


