Hvilke elementer reagerer klor med?
Metaller: Klor reagerer let med de fleste metaller til dannelse af metalchlorider . Disse reaktioner kan være ret kraftige, især med alkalimetaller som natrium og kalium. For eksempel:
* 2na + cl₂ → 2naCl (Natriumchlorid)
* fe + cl₂ → fecl₃ (Jern (III) chlorid)
ikke -metaller: Klor reagerer også med mange ikke -metaller og danner forskellige forbindelser:
* brint: Klor reagerer med brintgas til dannelse af hydrogenchlorid (HCI), en meget ætsende gas. Denne reaktion bruges ofte til at producere saltsyre.
* fosfor: Klor reagerer med fosfor til dannelse af fosforchlorider, såsom fosfortrichlorid (PCL₃) og phosphor -pentachlorid (PCL₅).
* svovl: Klor reagerer med svovl til dannelse af svovlchlorider, såsom svovldichlorid (SCL₂) og svovlmonochlorid (S₂CL₂).
* carbon: Klor reagerer med carbon for at danne carbontetrachlorid (CCL₄), et engang almindeligt opløsningsmiddel, men nu betragtes som skadeligt.
Andre reaktioner:
* Vand: Mens ikke strengt en reaktion med et element, reagerer klor med vand til dannelse af hypochlorosyre (HOCL) og saltsyre (HCI). Dette er grundlaget for klorens anvendelse i vanddesinfektion.
* organiske forbindelser: Klor kan reagere med organiske forbindelser på forskellige måder, hvilket fører til dannelse af chlorerede kulbrinter og andre produkter. Dette er grundlaget for mange industrielle kemiske processer, men bidrager også til miljøforurening.
Vigtig note: Mange af disse reaktioner er eksoterme (frigørelsesvarme) og kan være ret farlige. Det er vigtigt at håndtere klor og dets reaktioner med omhu og altid bære passende sikkerhedsudstyr.
Sidste artikelHvad er formlen for Plumbic Ion?
Næste artikelHvad er det stof, der bliver opløst?
 Varme artikler
Varme artikler
-
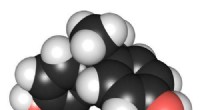 Nye katalysatorer fjerner effektivt og hurtigt BPA fra vand3D -kemisk struktur af bisphenol A. Kredit:Edgar181 via Wikimedia Commons Carnegie Mellon University -kemiker Terrence J. Collins har udviklet en tilgang, der hurtigt og billigt fjerner mere end 9
Nye katalysatorer fjerner effektivt og hurtigt BPA fra vand3D -kemisk struktur af bisphenol A. Kredit:Edgar181 via Wikimedia Commons Carnegie Mellon University -kemiker Terrence J. Collins har udviklet en tilgang, der hurtigt og billigt fjerner mere end 9 -
 Nyt bioremedieringsmateriale kan rense for evigt kemikalierPFAS adsorberes i plantematerialets cellevæg. Når svampen fortærer planten, spiser den også det kemikalie, der blev adsorberet. Kredit:Susie Dai En ny bioremedieringsteknologi til oprensning af per
Nyt bioremedieringsmateriale kan rense for evigt kemikalierPFAS adsorberes i plantematerialets cellevæg. Når svampen fortærer planten, spiser den også det kemikalie, der blev adsorberet. Kredit:Susie Dai En ny bioremedieringsteknologi til oprensning af per -
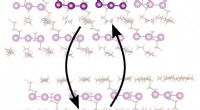 Nyt mellemprodukt opdaget til fotodissociation af triiodidanion, en klassisk lærebogsreaktionBilledet illustrerer fotodissociationen af triiodid initieret af en laserpuls og den sekundære reaktion, der fører til det nye 4-atom mellemprodukt, efterfulgt af rekombinationsreaktionen. Kredit:Bi
Nyt mellemprodukt opdaget til fotodissociation af triiodidanion, en klassisk lærebogsreaktionBilledet illustrerer fotodissociationen af triiodid initieret af en laserpuls og den sekundære reaktion, der fører til det nye 4-atom mellemprodukt, efterfulgt af rekombinationsreaktionen. Kredit:Bi -
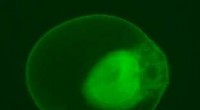 Enzymdrevne protoceller stiger til toppenFluorescensmikroskopibillede af en enzymholdig protocelle samlet af en blanding af DNA og lerpartikler. Kredit:Professor Stephen Mann, University of Bristol Forskere ved University of Bristol har
Enzymdrevne protoceller stiger til toppenFluorescensmikroskopibillede af en enzymholdig protocelle samlet af en blanding af DNA og lerpartikler. Kredit:Professor Stephen Mann, University of Bristol Forskere ved University of Bristol har
- Hvor mange grader Cecilius i en grad celsius?
- Hvorfor falske nyheder om coronavirus er tiltalende (og hvordan man undgår det)
- De længste levende stjerner er dem af?
- Første dybe boresucces for ExoMars
- Røg i ild kan bære mikrober, der forårsager infektionssygdomme
- Tag 2:Rumvandrende astronauter installerer nyt solpanel


