Hvad er den komplette ioniske ligning for bly II -nitrat og natriumsulfat?
1. Skriv den afbalancerede molekylære ligning:
Pb (no₃) ₂ (aq) + na₂so₄ (aq) → pbso₄ (s) + 2nano₃ (aq)
2. Identificer de opløselige ioniske forbindelser:
* Bly (ii) nitrat (Pb (no₃) ₂) er opløseligt i vand.
* Natriumsulfat (na₂so₄) er opløselig i vand.
* Bly (ii) sulfat (PBSO₄) er uopløseligt i vand (det danner et bundfald).
* Natriumnitrat (nano₃) er opløselig i vand.
3. Adskil de opløselige ioniske forbindelser i deres ioner:
* Pb (no₃) ₂ (aq) → pb²⁺ (aq) + 2no₃⁻ (aq)
* Na₂so₄ (aq) → 2na⁺ (aq) + so₄²⁻ (aq)
* PBSO₄ (r) forbliver som et fast stof.
* 2nano₃ (aq) → 2na⁺ (aq) + 2no₃⁻ (aq)
4. Kombiner ionerne for at danne den komplette ioniske ligning:
Pb²⁺ (aq) + 2no₃⁻ (aq) + 2na⁺ (aq) + so₄²⁻ (aq) → pbso₄ (s) + 2na⁺ (aq) + 2no₃⁻ (aq)
Dette er den komplette ioniske ligning.
Sidste artikelHvad er værdien af svovl?
Næste artikelHvad er balancen mellem siliciumreaktioner med kuldioxidform carbid og dioxid?
 Varme artikler
Varme artikler
-
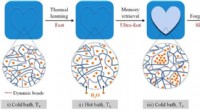 Hydrogel efterligner den menneskelige hjerne med evnen til at huske og glemmeHydrogelens huske-glemmende adfærd opnås baseret på hurtig vandoptagelse (hævelse) ved høj temperatur og langsom vandfrigivelse (krympning) ved lav temperatur, som er muliggjort af dynamiske bindinger
Hydrogel efterligner den menneskelige hjerne med evnen til at huske og glemmeHydrogelens huske-glemmende adfærd opnås baseret på hurtig vandoptagelse (hævelse) ved høj temperatur og langsom vandfrigivelse (krympning) ved lav temperatur, som er muliggjort af dynamiske bindinger -
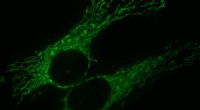 Bedre sammen:Mitokondriel fusion understøtter celledelingTo mitokondrier i en menneskelig celle. Kredit:Simon Troeder, Wikipedia Mitokondrier er cellens kraftværker. Og for mitokondrier, meget som for dobbelthovede motorer stablet sammen i et damptog, a
Bedre sammen:Mitokondriel fusion understøtter celledelingTo mitokondrier i en menneskelig celle. Kredit:Simon Troeder, Wikipedia Mitokondrier er cellens kraftværker. Og for mitokondrier, meget som for dobbelthovede motorer stablet sammen i et damptog, a -
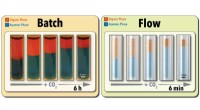 Grøn tilgang fremskynder procesoptimering og hentning af omskiftelige opløsningsmidlerKredit:North Carolina State University Forskere ved North Carolina State University har demonstreret en ny, grøn teknologi til både accelereret screening og hentning af omskiftelige opløsningsmidl
Grøn tilgang fremskynder procesoptimering og hentning af omskiftelige opløsningsmidlerKredit:North Carolina State University Forskere ved North Carolina State University har demonstreret en ny, grøn teknologi til både accelereret screening og hentning af omskiftelige opløsningsmidl -
 Isdannelse på overflader forstærket via en ikke-klassisk kernedannelsesprocesIskernedannelse på fremmede overflader kan forløbe via både et-trins (magenta pil) og to-trins (orange pile) veje, lettet af den afbalancerede synergetik, entropiske effekter af sekskantede (grønne ku
Isdannelse på overflader forstærket via en ikke-klassisk kernedannelsesprocesIskernedannelse på fremmede overflader kan forløbe via både et-trins (magenta pil) og to-trins (orange pile) veje, lettet af den afbalancerede synergetik, entropiske effekter af sekskantede (grønne ku
- Er vand og luft almindelige forbindelser?
- Hvad er det rigtige navn på sammensat fes?
- Hvad er Amber Stone?
- AI kan hjælpe med at forebygge kriminalitet, men vi har stadig brug for et menneske, der har ansvar…
- Amnesi, hvordan virker
- Kan mennesker og kunstig intelligens gå sammen for at forudsige fremtiden?


