Hvilken slags ioner bliver et natriumatom og klor, når valenselektron overføres fra hinanden?
* natrium (NA) Har en valenselektron i sin yderste skal. Den ønsker at miste dette elektron for at opnå en stabil oktet (8 elektroner) i sin yderste skal. Når det mister denne elektron, bliver det en positivt ladet ion kaldet en natriumkation (Na+) .
* klor (Cl) Har syv valenselektroner i sin yderste skal. Den ønsker at få et elektron for at opnå en stabil oktet. Når det får en elektron, bliver det en negativt ladet ion kaldet en chloridanion (Cl-) .
Kortfattet:
* natriumatom (NA) -> natriumkation (Na+)
* chloratom (CL)-> chlorid anion (CL-)
Sidste artikelHvor mange elektroniske orbitaler har dette atomchlor?
Næste artikelHvorfor ønsker klor at få 1 elektron?
 Varme artikler
Varme artikler
-
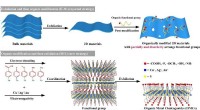 2-D-bestilte organiske metalchalcogenider udviklet med vidt indstillelige elektroniske båndgabSkematisk illustration af forskningen. Kredit:Prof. XUs gruppe To-dimensionelle (2-D) materialer, som viser fremragende fysiske og kemiske egenskaber, har modtaget hidtil uset opmærksomhed og er b
2-D-bestilte organiske metalchalcogenider udviklet med vidt indstillelige elektroniske båndgabSkematisk illustration af forskningen. Kredit:Prof. XUs gruppe To-dimensionelle (2-D) materialer, som viser fremragende fysiske og kemiske egenskaber, har modtaget hidtil uset opmærksomhed og er b -
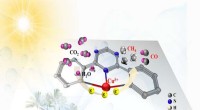 Ny katalysator øger radikalt omdannelseshastigheden af kuldioxid til solbrændstofferForskere konstruerede en enkelt atom katalysator (SAC) med en kovalent triazin-baseret ramme, hvormed fotokatalytisk CO2 blev omdannet til solenergi. Den fremstillede fotokatalysator udviste fremragen
Ny katalysator øger radikalt omdannelseshastigheden af kuldioxid til solbrændstofferForskere konstruerede en enkelt atom katalysator (SAC) med en kovalent triazin-baseret ramme, hvormed fotokatalytisk CO2 blev omdannet til solenergi. Den fremstillede fotokatalysator udviste fremragen -
 Saltning af omkostningerne ved proteinpolymerlægemidlerKredit:Carnegie Mellon University, Institut for Kemiteknik Protein er en stor forretning. Ikke alene udgør den en betydelig del af alle levende ting-det er også en industri på 150 milliarder dolla
Saltning af omkostningerne ved proteinpolymerlægemidlerKredit:Carnegie Mellon University, Institut for Kemiteknik Protein er en stor forretning. Ikke alene udgør den en betydelig del af alle levende ting-det er også en industri på 150 milliarder dolla -
 Uber medicin levering til kræftpatienterPh.d.-kandidaterne Samantha Wade og Sepehr Talebian, Dr Javad Foroughi, Fornemme professor Gordon Wallace og Dr. Kara Vine-Perrow. Kredit:Alex Pike Kræft er fortsat en af de største dødsårsager
Uber medicin levering til kræftpatienterPh.d.-kandidaterne Samantha Wade og Sepehr Talebian, Dr Javad Foroughi, Fornemme professor Gordon Wallace og Dr. Kara Vine-Perrow. Kredit:Alex Pike Kræft er fortsat en af de største dødsårsager


