Er der en reaktion mellem ammoniumchlorid og kaliumhydroxid?
Her er den afbalancerede kemiske ligning:
nh₄cl (aq) + KOH (aq) → Kcl (aq) + h₂o (l) + nh₃ (g)
Forklaring:
* nh₄cl er et surt salt, da det danner ammoniumioner (NH₄⁺) i opløsning, der fungerer som svage syrer.
* Koh er en stærk base, der leverer hydroxidioner (OH⁻) i opløsning.
* kcl er kaliumchlorid, et salt, der forbliver opløst i opløsningen.
* h₂o er vand, der produceres ved reaktionen af H⁺- og OH⁻ -ioner.
* nh₃ er ammoniakgas, der frigøres fra reaktionen.
Observationer:
* Reaktionen er eksoterm, hvilket betyder, at varme frigøres.
* En skarp lugt af ammoniakgas vil blive mærkbar.
* Løsningen kan blive overskyet på grund af dannelsen af ammoniakgasbobler.
Generelt resulterer reaktionen mellem ammoniumchlorid og kaliumhydroxid i dannelsen af kaliumchlorid, vand og ammoniakgas.
 Varme artikler
Varme artikler
-
 Instrumentet kan muliggøre mail-in test til at detektere tungmetaller i vandMIT -kandidatstuderende Emily Hanhauser demonstrerer en ny enhed, der kan forenkle logistikken ved vandovervågning for spormetalforureninger, især i ressourcebegrænsede regioner. Kredit:Melanie Gonick
Instrumentet kan muliggøre mail-in test til at detektere tungmetaller i vandMIT -kandidatstuderende Emily Hanhauser demonstrerer en ny enhed, der kan forenkle logistikken ved vandovervågning for spormetalforureninger, især i ressourcebegrænsede regioner. Kredit:Melanie Gonick -
 Jernbaserede solceller på vej til at blive mere effektiveKredit:CC0 Public Domain En international undersøgelse ledet fra Lunds Universitet i Sverige viser, at 30 procent af energien i en bestemt type lysabsorberende jernmolekyle forsvinder på en hidtil
Jernbaserede solceller på vej til at blive mere effektiveKredit:CC0 Public Domain En international undersøgelse ledet fra Lunds Universitet i Sverige viser, at 30 procent af energien i en bestemt type lysabsorberende jernmolekyle forsvinder på en hidtil -
 Stikkende smagsstof i ingefær reducerer dårlig åndeKredit:CC0 Public Domain Den skarpe forbindelse 6-gingerol, en bestanddel af ingefær, stimulerer et enzym i spyt, der nedbryder ildelugtende stoffer. Det sikrer dermed frisk ånde og en bedre efter
Stikkende smagsstof i ingefær reducerer dårlig åndeKredit:CC0 Public Domain Den skarpe forbindelse 6-gingerol, en bestanddel af ingefær, stimulerer et enzym i spyt, der nedbryder ildelugtende stoffer. Det sikrer dermed frisk ånde og en bedre efter -
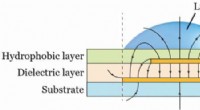 Hydrogel 3-D udskrivning og mønster af væsker med kondensatorkanteffekten (PLEEC)Princippet om PLEEC. En asymmetrisk kondensator er adskilt af et dielektrisk lag. Kredit:Science Advances, doi:10.1126/sciadv.aau8769 Hydrogeler er tredimensionelle (3-D) polymernetværk, der kan t
Hydrogel 3-D udskrivning og mønster af væsker med kondensatorkanteffekten (PLEEC)Princippet om PLEEC. En asymmetrisk kondensator er adskilt af et dielektrisk lag. Kredit:Science Advances, doi:10.1126/sciadv.aau8769 Hydrogeler er tredimensionelle (3-D) polymernetværk, der kan t


