Hvordan tester du, om brint er en gas?
Hvorfor brint er en gas:
* lav molekylvægt: Hydrogenmolekyler (H2) er utroligt lette. De har svage intermolekylære kræfter, hvilket gør det nemt for dem at bevæge sig frit og sprede sig.
* høj kinetisk energi: Ved stuetemperatur har brintmolekyler nok kinetisk energi til at overvinde disse svage kræfter, hvilket resulterer i en gasformig tilstand.
Observation af Hydrogen's gasformige natur:
1. visuel observation: Mens rent brint er farveløst og lugtfrit, kan du observere dens gasformige karakter gennem dens opførsel.
* diffusion: Brint diffunderer meget hurtigt, hvilket betyder, at det kan sprede sig hurtigt. Du kan demonstrere dette ved at fylde en ballon med brint og se den stige hurtigt på grund af dens lave tæthed.
* udvidelse: Hvis du lægger en lille mængde brint i en forseglet beholder, vil den fylde hele beholderen, når gassen udvides.
2. Kemisk reaktion:
* forbrænding: Hydrogen er meget brandfarligt. Hvis du udsætter brint for en flamme, vil det brænde med en lyseblå flamme og producere vanddamp. Denne forbrænding er en kemisk reaktion, men den viser tydeligt, at brint er en gas, der kan reagere og ændre tilstand.
3. Fysiske egenskaber:
* lav densitet: Hydrogen er det letteste element, så dens densitet som gas er ekstremt lav. Dette kan observeres ved at sammenligne opdriften af en ballon fyldt med brint med en ballon fyldt med luft.
* lavt kogepunkt: Hydrogen har et ekstremt lavt kogepunkt (-252,87 ° C eller -423,17 ° F). Dette betyder, at det allerede er en gas ved stuetemperatur.
Vigtige sikkerhedsnotater:
* Hydrogen er meget brandfarligt og kan være eksplosivt. Forsøg aldrig at skabe eller håndtere brint uden korrekt sikkerhedsudstyr og viden.
* Udfør kun eksperimenter med små mængder brint under omhyggeligt kontrollerede forhold.
Kortfattet: Du kan ikke "teste", hvis brint er en gas i traditionel forstand, da det allerede er en gas ved standardforhold. I stedet kan du observere dens karakteristiske gasformige opførsel gennem diffusion, ekspansion og kemiske reaktioner.
 Varme artikler
Varme artikler
-
 Kemikere opdager, hvordan blåt lys fremskynder blindhedDr. Ajith Karunarathne undersøgte giftig iltgenerering af retinal under eksponering for blåt lys. Kredit:Dan Miller, Universitetet i Toledo Blåt lys fra digitale enheder og solen forvandler vitale
Kemikere opdager, hvordan blåt lys fremskynder blindhedDr. Ajith Karunarathne undersøgte giftig iltgenerering af retinal under eksponering for blåt lys. Kredit:Dan Miller, Universitetet i Toledo Blåt lys fra digitale enheder og solen forvandler vitale -
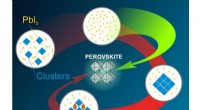 Kemikere bestemmer, hvordan man undgår biprodukter i syntesen af perovskitterRUDN -kemikere fandt ud af, hvordan man undgår biprodukter i syntesen af Perovskites Kredit:Natalia Deryugina En RUDN -professor, sammen med sine kolleger fra andre universiteter i Moskva, har b
Kemikere bestemmer, hvordan man undgår biprodukter i syntesen af perovskitterRUDN -kemikere fandt ud af, hvordan man undgår biprodukter i syntesen af Perovskites Kredit:Natalia Deryugina En RUDN -professor, sammen med sine kolleger fra andre universiteter i Moskva, har b -
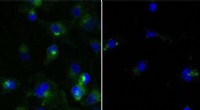 Cellulær oprydning kan også feje former for kræft vækCeller ubehandlet (venstre) eller behandlet (højre) med en PROTAC, der nedbryder målproteinet (grønt). Kredit:Yale University To nye forskningsartikler forstærker fordelene ved en ny terapi, der k
Cellulær oprydning kan også feje former for kræft vækCeller ubehandlet (venstre) eller behandlet (højre) med en PROTAC, der nedbryder målproteinet (grønt). Kredit:Yale University To nye forskningsartikler forstærker fordelene ved en ny terapi, der k -
 Forståelse af ødelæggelse og kvalitetsproblemer kan forbedre den amerikanske håndværker ostfrem…Eksempler på skorpedefekter omfatter (A) uønskede overfladeskimmel, såsom blåskimmel på camembert-ost (fotografi af B.E. Wolfe), (B) uønskede skorpefarver, såsom defekt lilla skorpe (Kamelamela et al.
Forståelse af ødelæggelse og kvalitetsproblemer kan forbedre den amerikanske håndværker ostfrem…Eksempler på skorpedefekter omfatter (A) uønskede overfladeskimmel, såsom blåskimmel på camembert-ost (fotografi af B.E. Wolfe), (B) uønskede skorpefarver, såsom defekt lilla skorpe (Kamelamela et al.


