Hvordan er to isotoper af et element ens?
* samme antal protoner: Isotoper er atomer med det samme element, hvilket betyder, at de har det samme antal protoner, der bestemmer elementets atomnummer. Det er det, der gør dem til det samme element.
* samme kemiske egenskaber: På grund af at have det samme antal protoner og elektroner udviser isotoper typisk lignende kemiske egenskaber. De reagerer på lignende måde i kemiske reaktioner.
* samme antal elektroner: Isotoper har det samme antal elektroner som protoner, hvilket sikrer en neutral ladning. Dette er grunden til, at de deler lignende kemisk opførsel.
Her er en analogi: Forestil dig, at du har to tvillinger. De deler det samme DNA (protoner) og ser meget ens ud (elektroner). Men den ene tvilling er måske lidt tungere end den anden (neutroner). Denne forskel i vægt er som forskellen i neutroner mellem isotoper.
Isotoper adskiller sig imidlertid i følgende:
* Antal neutroner: Isotoper har et andet antal neutroner, der påvirker deres atommasse.
* atommasse: Fordi de har forskellige antal neutroner, har isotoper forskellige atommasser.
* Fysiske egenskaber: Forskelle i neutronantal kan lidt påvirke de fysiske egenskaber ved isotoper, såsom densitet, smeltepunkt og kogepunkt.
Kortfattet: Mens isotoper af et element deler den samme kemiske opførsel på grund af identiske proton- og elektronoptællinger, adskiller de sig i deres atommasse og nogle fysiske egenskaber på grund af variationer i deres neutronantal.
 Varme artikler
Varme artikler
-
 At finde grønne opløsningsmidler til trykt elektronikFysikforskere har udviklet og offentliggjort et åbent webværktøj til let identifikation af grønne opløsningsmidler til trykt elektronik. Kredit:Joan Ràfols-Ribé Det nye felt inden for trykt elektr
At finde grønne opløsningsmidler til trykt elektronikFysikforskere har udviklet og offentliggjort et åbent webværktøj til let identifikation af grønne opløsningsmidler til trykt elektronik. Kredit:Joan Ràfols-Ribé Det nye felt inden for trykt elektr -
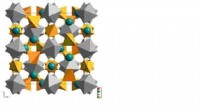 Oprettelse af et nyt kompositbrændstof til næste generations hurtige reaktorerKrystalstrukturen af yttrium-aluminium granat. Kredit:Lobachevsky University Fælles forskningsindsats af et team af videnskabsmænd ved Lobachevsky University of Nizhny Novgorod (UNN), bestående
Oprettelse af et nyt kompositbrændstof til næste generations hurtige reaktorerKrystalstrukturen af yttrium-aluminium granat. Kredit:Lobachevsky University Fælles forskningsindsats af et team af videnskabsmænd ved Lobachevsky University of Nizhny Novgorod (UNN), bestående -
 Modificeret svamp kunne genvinde olieforurenende stoffer fra arktiske farvandeKredit:Unsplash/CC0 Public Domain Forskere har udviklet en bæredygtig og økonomisk måde at genvinde olie fra ultrakoldt industrielt spildevand og olieudslip. Forskere fra Imperial College London
Modificeret svamp kunne genvinde olieforurenende stoffer fra arktiske farvandeKredit:Unsplash/CC0 Public Domain Forskere har udviklet en bæredygtig og økonomisk måde at genvinde olie fra ultrakoldt industrielt spildevand og olieudslip. Forskere fra Imperial College London -
 Forskere afslører det molekylære grundlag for synKredit:CC0 Public Domain Forskere har løst den tredimensionelle struktur af et proteinkompleks involveret i hvirveldyrs syn ved atomopløsning, et fund, der har brede implikationer for vores forstå
Forskere afslører det molekylære grundlag for synKredit:CC0 Public Domain Forskere har løst den tredimensionelle struktur af et proteinkompleks involveret i hvirveldyrs syn ved atomopløsning, et fund, der har brede implikationer for vores forstå


