Hvorfor reagerer ikke aluminium med hyrdochlorsyrer?
Her er hvorfor:
* aluminium er et reaktivt metal: Det reagerer let med syrer, herunder saltsyre (HCI).
* reaktionsproces: Reaktionen producerer aluminiumchlorid (ALCL3) og brintgas (H2). Den kemiske ligning for denne reaktion er:
2al (s) + 6HCl (aq) → 2Alcl3 (aq) + 3H2 (g)
* Observation: Når du placerer aluminium i saltsyre, ser du bobler af brintgasformning og aluminiumsmetalopløsning.
Hvorfor kan der være forvirring:
* aluminiumoxidlag: Aluminium har et tyndt, beskyttende lag af aluminiumoxid (Al2O3) på dens overflade. Dette lag er relativt ureaktivt og kan forhindre yderligere reaktion med svage syrer.
* Koncentreret syre: Med meget koncentreret saltsyre kan reaktionen nedsættes eller endda stoppes på grund af dannelsen af et beskyttende lag af aluminiumchlorid.
Kortfattet: Aluminium reagerer med saltsyre, men reaktionshastigheden kan påvirkes af faktorer som koncentrationen af syren og tilstedeværelsen af aluminiumoxidlaget.
Sidste artikelHvor mange carbonatomer er der i molekylets hexan?
Næste artikelHvorfor danner hexan ikke en opløsning med vand?
 Varme artikler
Varme artikler
-
 Nøglen til at udvide genetisk kode beskrevetEn illustration af biokemisk sammensætning af pyrrolysyl-tRNA syntetase (PylRS) kompleks, en af nøglerne til at udvide den genetiske kode. Kredit:Yale University Yale -forskere har beskrevet ato
Nøglen til at udvide genetisk kode beskrevetEn illustration af biokemisk sammensætning af pyrrolysyl-tRNA syntetase (PylRS) kompleks, en af nøglerne til at udvide den genetiske kode. Kredit:Yale University Yale -forskere har beskrevet ato -
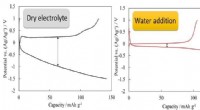 Elektrolyttens struktur styrer batteriets ydeevneVi har fundet ud af, at tilsætning af vand i høj grad reducerer forskellen i spænding (overspænding) mellem opladning/afladning. Kredit:COPYRIGHT (C) TOYOHASHI UNIVERSITY OF TECHNOLOGY. Forskerhol
Elektrolyttens struktur styrer batteriets ydeevneVi har fundet ud af, at tilsætning af vand i høj grad reducerer forskellen i spænding (overspænding) mellem opladning/afladning. Kredit:COPYRIGHT (C) TOYOHASHI UNIVERSITY OF TECHNOLOGY. Forskerhol -
 Enzymdrevne protoceller stiger til toppenFluorescensmikroskopibillede af en enzymholdig protocelle samlet af en blanding af DNA og lerpartikler. Kredit:Professor Stephen Mann, University of Bristol Forskere ved University of Bristol har
Enzymdrevne protoceller stiger til toppenFluorescensmikroskopibillede af en enzymholdig protocelle samlet af en blanding af DNA og lerpartikler. Kredit:Professor Stephen Mann, University of Bristol Forskere ved University of Bristol har -
 Meget følsom trigger muliggør hurtig påvisning af biologiske agenserRapid Agent Aerosol Detector blev fotograferet med en 12-tommer lineal for at illustrere skalaen. Kredit:Massachusetts Institute of Technology Enhver plads, lukket eller åben, kan være sårbare ove
Meget følsom trigger muliggør hurtig påvisning af biologiske agenserRapid Agent Aerosol Detector blev fotograferet med en 12-tommer lineal for at illustrere skalaen. Kredit:Massachusetts Institute of Technology Enhver plads, lukket eller åben, kan være sårbare ove
- Hvorfor en astronomer fungerer er vigtig?
- Hvad hedder bunden af en dal?
- Hvordan AI former fremtiden for salgsstrategier
- Infografik:Sådan mister du ikke et rumfartøj
- Verizon afslutter salget af datadata til mæglere
- Hvad er den afbalancerede ligning, der beskriver reaktion mellem brintgas og nitrogen til at produce…


