Hvorfor har natrium og klor så forskellige egenskaber, når de findes som elementer fra forbindelseschloridet?
Her er en sammenbrud:
natrium (NA) som et element:
* Metallic: Skinnende, sølvhvid, blødt og meget reaktivt metal.
* Meget reaktiv: Mister let en elektron for at opnå en stabil elektronkonfiguration.
* farlig: Meget brandfarlig og reagerer voldsomt med vand.
klor (CL) som et element:
* gasformig: En grønlig-gul, skarp og giftig gas.
* Meget reaktiv: Få en elektron let for at opnå en stabil elektronkonfiguration.
* farlig: Kan forårsage luftvejsproblemer og er et kraftfuldt oxidationsmiddel.
natriumchlorid (NaCl) som en forbindelse:
* ionisk: Et krystallinsk fast stof med et højt smeltepunkt.
* ikke-reaktiv: Relativt ureaktiv og stabil sammenlignet med dens bestanddele.
* essentiel: Vigtigt for livet og findes i bordsalt.
Den vigtigste forskel:
Den dramatiske ændring i egenskaber skyldes ionisk binding . Natrium og klor danner en ionisk forbindelse ved at overføre elektroner:
* Natrium (NA) mister et elektron for at blive et positivt ladet natriumion (Na+).
* Chlor (CL) får det elektron til at blive en negativt ladet chloridion (Cl-).
Disse modsatte ladede ioner tiltrækkes af hinanden gennem elektrostatiske kræfter og danner en stærk ionisk binding. Denne binding skaber en ny struktur og ændrer markant de kemiske og fysiske egenskaber ved den resulterende forbindelse.
Sådan manifesteres ændringen i egenskaber:
* reaktivitet: Natrium og klor er begge stærkt reaktive elementer, men deres reaktivitet neutraliseres i NaCl. Den ioniske binding gør forbindelsen meget mere stabil.
* tilstand: Det bløde, metalliske natrium og gasformige klor danner et hårdt, krystallinsk fast stof.
* udseende: Den metalliske glans af natrium og den grønne gas af klor forsvinder i den hvide, gennemskinnelige natriumchlorid.
* toksicitet: De farlige egenskaber ved både natrium og klor mindskes i det ikke-toksiske natriumchlorid.
I det væsentlige involverer dannelsen af natriumchlorid en grundlæggende kemisk transformation, der drastisk ændrer opførslen og egenskaberne for de bestanddele.
Sidste artikelHvor rigeligt er brint?
Næste artikelHvad er formlen for mangan II acetat?
 Varme artikler
Varme artikler
-
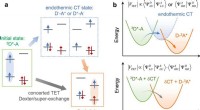 Endoterm ladningsoverførsel medierer overfladeafstandsafhængig trilling energimigrationen skematisk afbildning af de indledende og endelige tilstande og mellemliggende endoterme CT -tilstande. 3D* -A og D-3A* er de indledende og sidste tilstande, henholdsvis, der henviser til, at D −- A
Endoterm ladningsoverførsel medierer overfladeafstandsafhængig trilling energimigrationen skematisk afbildning af de indledende og endelige tilstande og mellemliggende endoterme CT -tilstande. 3D* -A og D-3A* er de indledende og sidste tilstande, henholdsvis, der henviser til, at D −- A -
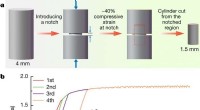 Foryngende metallisk glas for at forhindre brudForyngelse og deformation af en MG. Kredit: Natur (2020). DOI:10.1038/s41586-020-2016-3 Et team af forskere fra det kinesiske videnskabsakademi og University of Cambridge har fundet en måde at fo
Foryngende metallisk glas for at forhindre brudForyngelse og deformation af en MG. Kredit: Natur (2020). DOI:10.1038/s41586-020-2016-3 Et team af forskere fra det kinesiske videnskabsakademi og University of Cambridge har fundet en måde at fo -
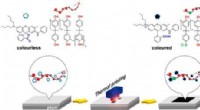 Et skridt i retning af at kvitte register kvitteringer af BPAKredit:American Chemical Society Selvom USA og andre lande har forbudt eller begrænset brugen af bisphenol A (BPA) på grund af miljø- og sundhedsmæssige bekymringer, det bruges stadig i termotry
Et skridt i retning af at kvitte register kvitteringer af BPAKredit:American Chemical Society Selvom USA og andre lande har forbudt eller begrænset brugen af bisphenol A (BPA) på grund af miljø- og sundhedsmæssige bekymringer, det bruges stadig i termotry -
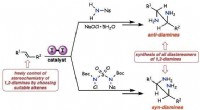 Molekylært jod katalyserer processer til antivirale og farmaceutiske synteserFigur 1. Skematisk diagram af anti- og syn-diamineringerne af alkener ved anvendelse af jodkatalysator. Kredit:Osaka University Syntetisering af lægemidler til kræft, virale sygdomme, og andre med
Molekylært jod katalyserer processer til antivirale og farmaceutiske synteserFigur 1. Skematisk diagram af anti- og syn-diamineringerne af alkener ved anvendelse af jodkatalysator. Kredit:Osaka University Syntetisering af lægemidler til kræft, virale sygdomme, og andre med
- Hvad er betydningen af lys stjerne i den østlige himmel nordlige halvkugle?
- Brugte biler holder afrikanere i gang, men der er stadig bekymringer for dumping
- Udnyttelse af helt dielektriske metamaterialer til at manipulere lysets polarisationstilstand
- Forståelse af ladningspumpning og afslapning af den chirale anomali i en Dirac semimetal
- Apple-aktien falder efter skuffende ferieudsigter
- Hvordan fungerer chromotograhy ved hjælp af partikler?


