Hvad er den molære masse af svovlmolekyle?
* octasulfur (s 8 ): Dette er den mest stabile form for svovl ved stuetemperatur. Det har en molær masse på:
* 8 Svovlatomer * 32,065 g/mol pr. Svovlatom = 256,52 g/mol
Andre former for svovl:
* s 2 : Har en molær masse på 2 * 32,065 g/mol =64,13 g/mol.
* s 6 : Har en molær masse på 6 * 32,065 g/mol =192,39 g/mol.
Derfor er det vigtigt at kende det specifikke svovlmolekyle, du arbejder med for at bestemme dets molære masse. for den mest almindelige form, S 8 , den molære masse er 256,52 g/mol.
Sidste artikelHvorfor er symbolet for element svovl forskellig fra formel A -molekyle af svovl?
Næste artikelHvad er natriummethylsulfat?
 Varme artikler
Varme artikler
-
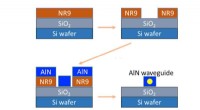 Forskere reducerer drastisk teknologi til fingeraftryk af lægemidler og andre kemikalierSkematisk, der viser trinene til oprettelse af den optiske bølgeleder. Kredit:Texas A&M University College of Engineering Efterhånden som nye infektionssygdomme opstår og spredes, et af de bedste
Forskere reducerer drastisk teknologi til fingeraftryk af lægemidler og andre kemikalierSkematisk, der viser trinene til oprettelse af den optiske bølgeleder. Kredit:Texas A&M University College of Engineering Efterhånden som nye infektionssygdomme opstår og spredes, et af de bedste -
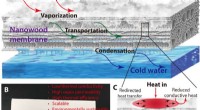 Ny træmembran giver et bæredygtigt alternativ til vandfiltreringSkematisk af processen med brug af den nye træmembran til destillering af vand. Kredit:T. Li, University of Maryland. Inspireret af det indviklede vandsystem, der cirkulerer i et træ, et team af f
Ny træmembran giver et bæredygtigt alternativ til vandfiltreringSkematisk af processen med brug af den nye træmembran til destillering af vand. Kredit:T. Li, University of Maryland. Inspireret af det indviklede vandsystem, der cirkulerer i et træ, et team af f -
 Genbrug af 1 kg tøj sparer 25 kg CO2, viser undersøgelseEn stigning på 10 % i brugtsalg kan spare 3 % af CO2-udledningen og 4 % af vandet. Kredit:Moda re- (Cáritas) UPCs INTEXTER har foretaget en analyse for at beregne andelen af fibre, der bruges i d
Genbrug af 1 kg tøj sparer 25 kg CO2, viser undersøgelseEn stigning på 10 % i brugtsalg kan spare 3 % af CO2-udledningen og 4 % af vandet. Kredit:Moda re- (Cáritas) UPCs INTEXTER har foretaget en analyse for at beregne andelen af fibre, der bruges i d -
 Molekylær kortlægning gjort let3D-kort over molekylerne på en pengeautomat. Dette kort viser, hvordan vi overfører molekyler fra vores hud til de objekter, vi interagerer med, give oplysninger, der kan have mange retsmedicinske anv
Molekylær kortlægning gjort let3D-kort over molekylerne på en pengeautomat. Dette kort viser, hvordan vi overfører molekyler fra vores hud til de objekter, vi interagerer med, give oplysninger, der kan have mange retsmedicinske anv
- Hvilke mikrober lever i din tarm? En mikrobiolog prøver hjemme-testsæt for at se, hvad de afsløre…
- Hvordan navneændring kan påvirke en kvindelig forskerkarriere
- Majs bedre brugt som mad end biobrændstof, undersøgelse finder
- David vs. Goliat:Hvad en lille elektron kan fortælle os om universets struktur
- Hvad er de 5 principper for partikelteorien noget?
- Sådan fungerer lyspinde


