Hvad er formlen for ion, der dannes, når svovl opnår en ædelgaselektronkonfiguration?
* Svovls elektronkonfiguration: Svovl (er) har et atomnummer på 16, hvilket betyder, at det har 16 elektroner. Dens elektronkonfiguration er 1S² 2S²2P⁶3S²3P⁴.
* ædle gaskonfiguration: Den nærmeste ædle gas til svovl er argon (AR), som har en elektronkonfiguration på 1S² 2S²2p⁶3S²3p⁶.
* At vinde elektroner: For at opnå den samme elektronkonfiguration som argon skal svovl få to flere elektroner. Dette vil fylde sin 3P -underskal.
* iondannelse: Når svovl får to elektroner, bliver det negativt ladet og danner sulfidionen (S²⁻).
Derfor er formlen for den ion, der er dannet, når svovl opnår en ædelgaselektronkonfiguration er s²⁻.
Sidste artikelHvad vil påvirke elektrolysen af smeltet kobberchlorid?
Næste artikelDen fulde elektronkonfiguration til svovlatom?
 Varme artikler
Varme artikler
-
 Verdens ældste periodiske diagram fundet i St. AndrewsPeriodisk bordvaskebehandling. Kredit:University of St. Andrews Et periodisk tabeldiagram opdaget ved University of St Andrews menes at være det ældste i verden. Diagrammet af elementer, stammer
Verdens ældste periodiske diagram fundet i St. AndrewsPeriodisk bordvaskebehandling. Kredit:University of St. Andrews Et periodisk tabeldiagram opdaget ved University of St Andrews menes at være det ældste i verden. Diagrammet af elementer, stammer -
 Værktøjssæt:Brug af lokal jord til 3D-print af store strukturer(A) Illustration af geopolymerisationstilgang udviklet til at størkne moskus til en bærende silikatkomposit, som repræsenteret ved kraften af et bildæk på vej forstærket af kompositmaterialet, genop
Værktøjssæt:Brug af lokal jord til 3D-print af store strukturer(A) Illustration af geopolymerisationstilgang udviklet til at størkne moskus til en bærende silikatkomposit, som repræsenteret ved kraften af et bildæk på vej forstærket af kompositmaterialet, genop -
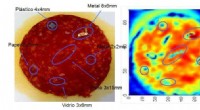 Design af sensorer til at detektere fremmedlegemer i fødevarerBillede opnået med denne teknologi, hvor der kan ses, på et stykke pølse, plast, metaller og splinter af glas i forskellige størrelser og former. Kredit:Elhuyar Fundazioa Forskere ved NUP/UPNA-Pub
Design af sensorer til at detektere fremmedlegemer i fødevarerBillede opnået med denne teknologi, hvor der kan ses, på et stykke pølse, plast, metaller og splinter af glas i forskellige størrelser og former. Kredit:Elhuyar Fundazioa Forskere ved NUP/UPNA-Pub -
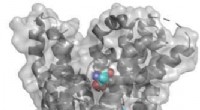 Proteinernæring til celler og organismer:Kan vi bruge det til behandling af sygdomme?Bindingsstedet for EAAT1-hæmmeren (UCPH101) opløses ved røntgenkrystallografi og er placeret i en afstand fra substratbindingsstedet. Substratet er vist i midten af transportøren, mens inhibitoren e
Proteinernæring til celler og organismer:Kan vi bruge det til behandling af sygdomme?Bindingsstedet for EAAT1-hæmmeren (UCPH101) opløses ved røntgenkrystallografi og er placeret i en afstand fra substratbindingsstedet. Substratet er vist i midten af transportøren, mens inhibitoren e
- Det svarer til en ny kvantevæske?
- Hvilken type klipper dannes gennem processen opvarmning og afkøling under overfladen?
- Quantum dot solids:Denne generation af siliciumwafer?
- Ny enhed lagrer elektricitet på siliciumchips
- Hvad er Hubble-teleskopet, og hvordan hjælper det os?
- Puster nyt liv i eksisterende teknologi:FT-IR-spektrometer viser molekylær orientering


