Den fulde elektronkonfiguration til svovlatom?
1S² 2S² 2P⁶ 3S² 3P⁴
Her er en sammenbrud:
* 1S²: Det første energiniveau (n =1) har et underskal, 'S' underskalet, der kan holde op til 2 elektroner.
* 2s²: Det andet energiniveau (n =2) har også et 'S' underskal med 2 elektroner.
* 2p⁶: Det andet energiniveau har også et 'P' underskal, der kan holde op til 6 elektroner.
* 3S²: Det tredje energiniveau (n =3) har et 'S' underskal med 2 elektroner.
* 3p⁴: Det tredje energiniveau har også et 'P' underskal med 4 elektroner.
Denne konfiguration viser fordelingen af svovlens 16 elektroner på tværs af dets forskellige energiniveauer og underskaller.
 Varme artikler
Varme artikler
-
 Bionedbrydelige plantebeskyttelsesmidler uden risici eller bivirkningerEt hold fra det tekniske universitet i München (TUM) har udviklet et biologisk nedbrydeligt middel, der holder skadedyr på afstand uden at forgifte dem:som myggemiddel, der bruges af badende om sommer
Bionedbrydelige plantebeskyttelsesmidler uden risici eller bivirkningerEt hold fra det tekniske universitet i München (TUM) har udviklet et biologisk nedbrydeligt middel, der holder skadedyr på afstand uden at forgifte dem:som myggemiddel, der bruges af badende om sommer -
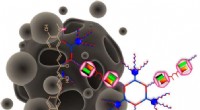 Forskere opdager metode til at levere urtetilskud curcumin til kræftceller ved at løse dets uoplø…Holdet detaljerede en hierarkisk tilgang til at solubilisere et hydrofobt anti-cancer lægemiddel, curcumin i vand via en kombination af koordinationsdrevet selvsamling og vært-gæst interaktioner. Kred
Forskere opdager metode til at levere urtetilskud curcumin til kræftceller ved at løse dets uoplø…Holdet detaljerede en hierarkisk tilgang til at solubilisere et hydrofobt anti-cancer lægemiddel, curcumin i vand via en kombination af koordinationsdrevet selvsamling og vært-gæst interaktioner. Kred -
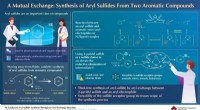 Syntetisering af arylsulfider fra ikke-lugtende, ikke-giftige forbindelserNi-katalyseret arylsulfidsyntese gennem en arylbytningsreaktion. Kredit:Waseda University Arylsulfid, en aromatisk forbindelse, hvor svovl er bundet til en aryl (en funktionel gruppe afledt af en
Syntetisering af arylsulfider fra ikke-lugtende, ikke-giftige forbindelserNi-katalyseret arylsulfidsyntese gennem en arylbytningsreaktion. Kredit:Waseda University Arylsulfid, en aromatisk forbindelse, hvor svovl er bundet til en aryl (en funktionel gruppe afledt af en -
 Ny elektrokatalysator udkonkurrerer platin i produktionen af alkalisk brintDen nye katalysator er et nanostruktureret kompositmateriale sammensat af carbon nanotråde med rutheniumatomer bundet til nitrogen og carbon for at danne aktive steder i carbonmatrixen. Elektronmikros
Ny elektrokatalysator udkonkurrerer platin i produktionen af alkalisk brintDen nye katalysator er et nanostruktureret kompositmateriale sammensat af carbon nanotråde med rutheniumatomer bundet til nitrogen og carbon for at danne aktive steder i carbonmatrixen. Elektronmikros
- Hvad er de nødvendige betingelser for at vise årsagssammenhæng i videnskaben?
- Hvordan afgør du, om ligningen er afbalanceret?
- Høj bjergkæde i det vestlige USA?
- Hvilken forvitringsproces er resultatet af fjernelse af mineraler i jordens sten?
- I Rusland, legenden om kosmonauten Gagarin lever videre
- Kunne Iron Man -stil passer være svaret på verdens største atomudfordring?


