Hvor mange elektroner skal svovl være en stabil oktet?
Her er hvorfor:
* Svovls elektronkonfiguration: Svovl har 16 elektroner med følgende konfiguration:2, 8, 6. Dette betyder, at det har 6 elektroner i sin yderste skal (Valence Shell).
* octet regel: Octet -reglen siger, at atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration af 8 elektroner i deres yderste skal.
* Svovls behov: Svovl har brug for yderligere 2 elektroner for at fylde sin yderste skal og opnå den stabile oktetkonfiguration.
Dette er grunden til, at svovl ofte danner forbindelser, hvor det har en -2 -ladning, hvilket betyder gevinsten for to elektroner.
Sidste artikelDen fulde elektronkonfiguration til svovlatom?
Næste artikelHvad er jordtilstandens elektronkonfiguration af element svovl?
 Varme artikler
Varme artikler
-
 Papirspor fører til hjerteklap opdagelserRisforskere konfigurerer lagdelt filterpapir til at efterligne aorta-hjerteklapper. Kredit:Jeff Fitlow Papir er kernen i en eksperimentel enhed udviklet af Rice University bioingeniører til at stu
Papirspor fører til hjerteklap opdagelserRisforskere konfigurerer lagdelt filterpapir til at efterligne aorta-hjerteklapper. Kredit:Jeff Fitlow Papir er kernen i en eksperimentel enhed udviklet af Rice University bioingeniører til at stu -
 Kobber-indiumoxid:En hurtigere og køligere måde at reducere vores CO2-fodaftrykEn rekordhøj CO 2 konverteringshastigheder ved relativt lave temperaturer i en modificeret version af RWGS med kemisk sløjfe ved hjælp af et nyt kobber-indiumoxid Kredit:Waseda University Med st
Kobber-indiumoxid:En hurtigere og køligere måde at reducere vores CO2-fodaftrykEn rekordhøj CO 2 konverteringshastigheder ved relativt lave temperaturer i en modificeret version af RWGS med kemisk sløjfe ved hjælp af et nyt kobber-indiumoxid Kredit:Waseda University Med st -
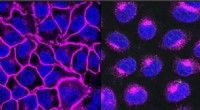 Kemikere laver molekylære skalpeller for at fjerne uønskede proteiner fra celleoverfladerEGFR, et protein, der er vigtigt for at hjælpe kræftformer med at vokse, vist her i lilla, dekorerer celleoverfladen (venstre). Efter behandling med en EGFR-målrettet LYTAC, alt EGFR-protein transport
Kemikere laver molekylære skalpeller for at fjerne uønskede proteiner fra celleoverfladerEGFR, et protein, der er vigtigt for at hjælpe kræftformer med at vokse, vist her i lilla, dekorerer celleoverfladen (venstre). Efter behandling med en EGFR-målrettet LYTAC, alt EGFR-protein transport -
 Mekaniske ingeniører udvikler proces til 3-D-print af piezoelektriske materialerEt trykt fleksibelt ark af piezoelektrisk smart materiale Kredit:H. Cui fra Zheng Lab De piezoelektriske materialer, der bebor alt fra vores mobiltelefoner til musikalske lykønskningskort, får mul
Mekaniske ingeniører udvikler proces til 3-D-print af piezoelektriske materialerEt trykt fleksibelt ark af piezoelektrisk smart materiale Kredit:H. Cui fra Zheng Lab De piezoelektriske materialer, der bebor alt fra vores mobiltelefoner til musikalske lykønskningskort, får mul
- Hvilket element er flydende metal?
- Hvis en fugl forlader fodaftryk i mudderet hærder, hvilken slags fossil er dette?
- Sedimentære klipper, der består af store småsten og sten, har en grovkornet?
- Fleksibel elektronisk hud hjælper mennesker-maskine interaktioner
- Hvorfor er hydrogenbinding ikke til stede i sulfid?
- Hvordan kan brug af loven om bevaringsmasse til at hjælpe dig med at afbalancere en kemisk ligning?…


