Hvis klorgas bobles gennem en vandig opløsning af natriumiodid, resultatet Elementær jod og chlorid, hvilken slags reaktion fandt sted?
* enkelt forskydning: I denne type reaktion fortrænger et mere reaktivt element et mindre reaktivt element fra dets forbindelse.
* reaktionen: Klor (CL₂) er mere reaktiv end jod (I₂). Når klorgas bobles gennem en opløsning af natriumiodid (NAI), fortrænger kloratomerne iodatomerne fra iodidionerne (I⁻).
Den kemiske ligning:
Cl₂ (G) + 2NAI (AQ) → 2NACL (AQ) + I₂ (S)
* reaktanter: Klorgas (CL₂) og natriumiodid (NAI)
* Produkter: Natriumchlorid (NaCl) og elementær jod (I₂)
Forklaring:
* Chlor (CL₂) er et stærkere oxidationsmiddel end jod (I₂). Dette betyder, at det har en større tendens til at få elektroner.
* Chloratomer reagerer med iodidioner (I⁻) for at danne chloridioner (CL⁻) og elementært iod (I₂).
* Jodatomerne kombineres derefter for at danne diatomiske jodmolekyler (I₂), som er uopløselige i vand og udfælder som et fast stof.
Nøglepunkter:
* Reaktionen er drevet af forskellen i reaktivitet mellem klor og jod.
* Reaktionen producerer en farveændring, da den farveløse opløsning bliver brun på grund af dannelsen af elementær jod.
 Varme artikler
Varme artikler
-
 Fremstillingen af en krystalflipperKredit:CC0 Public Domain Forskere fra Hokkaido-universitetet har fremstillet en krystal, der automatisk vipper frem og tilbage, mens de ændrer sine vendemønstre som reaktion på lysforholdene. Dere
Fremstillingen af en krystalflipperKredit:CC0 Public Domain Forskere fra Hokkaido-universitetet har fremstillet en krystal, der automatisk vipper frem og tilbage, mens de ændrer sine vendemønstre som reaktion på lysforholdene. Dere -
 En bæredygtig ny løsning til aldring, korroderende infrastrukturNy forskning ved UC ledet af strukturingeniørprofessor Alessandro Palermo (til højre) har fremhævet den indvirkning, forringelse kan have på konstruktioners ydeevne. Ph.d.-studerende Cain Stratford (t
En bæredygtig ny løsning til aldring, korroderende infrastrukturNy forskning ved UC ledet af strukturingeniørprofessor Alessandro Palermo (til højre) har fremhævet den indvirkning, forringelse kan have på konstruktioners ydeevne. Ph.d.-studerende Cain Stratford (t -
 Lyser vejen til forbedrede biomaterialerKredit:Sleiman Lab Forskere fra McGill University mener, at de har fundet en måde at forbedre udviklingen af biomaterialer, der kunne være medvirkende til lægemiddellevering, vævsregenerering, n
Lyser vejen til forbedrede biomaterialerKredit:Sleiman Lab Forskere fra McGill University mener, at de har fundet en måde at forbedre udviklingen af biomaterialer, der kunne være medvirkende til lægemiddellevering, vævsregenerering, n -
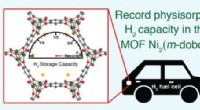 Baner vejen for mere effektive brintbilerKredit:American Chemical Society Brintdrevne køretøjer udsender kun vanddamp fra deres udstødningsrør, at tilbyde et renere alternativ til fossilt brændstof-baseret transport. Men for at brintbile
Baner vejen for mere effektive brintbilerKredit:American Chemical Society Brintdrevne køretøjer udsender kun vanddamp fra deres udstødningsrør, at tilbyde et renere alternativ til fossilt brændstof-baseret transport. Men for at brintbile


