Natrium og kalium har lignende kemiske fysiske egenskaber, denne observation er bedst forklaret af det faktum, at begge elementer?
* Elektronkonfiguration: Elementer i den samme gruppe har det samme antal valenselektroner (elektroner i den yderste skal). Natrium og kalium har begge en valenselektron. Denne lignende elektronkonfiguration er den primære årsag til deres delte egenskaber.
* reaktivitet: Med en valenselektron mister både natrium og kalium let det elektron til dannelse af en +1 kation, hvilket gør dem meget reaktive metaller.
* Metallisk binding: Begge elementer danner metalliske bindinger, hvilket resulterer i deres karakteristiske formbarhed, duktilitet og god ledningsevne.
Derfor er svaret:Begge elementer har det samme antal valenselektroner.
 Varme artikler
Varme artikler
-
 Ny test identificerer giftige svampeSpiselige og giftige svampe indsamlet fra naturen kan være svære at skelne fra hinanden. Kredit:Candace Bever, ARS-USDA En enkel, bærbar test, der kan påvise den dødeligste af svampegiftene på få
Ny test identificerer giftige svampeSpiselige og giftige svampe indsamlet fra naturen kan være svære at skelne fra hinanden. Kredit:Candace Bever, ARS-USDA En enkel, bærbar test, der kan påvise den dødeligste af svampegiftene på få -
 Kemikere varmer op til preprint-servereKredit:Charles Rondeau/public domain Preprint-servere – onlinewebsteder, der sender videnskabelige manuskripter gratis, forud for peer review-er veletablerede inden for områder som fysik og biolog
Kemikere varmer op til preprint-servereKredit:Charles Rondeau/public domain Preprint-servere – onlinewebsteder, der sender videnskabelige manuskripter gratis, forud for peer review-er veletablerede inden for områder som fysik og biolog -
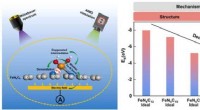 Forskere afslører nedbrydningsmekanismen for ikke-ædelmetalkatalysatorer til brændselscellerGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121290 Udviklingen af effektive ikke-ædelmetalkatalysatorer (NPMCer) kan hjælpe med at reducere omkostningerne
Forskere afslører nedbrydningsmekanismen for ikke-ædelmetalkatalysatorer til brændselscellerGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121290 Udviklingen af effektive ikke-ædelmetalkatalysatorer (NPMCer) kan hjælpe med at reducere omkostningerne -
 Gennemsigtigt træ:fremtidens byggemateriale?Gennemsigtigt træ skabes ved at fjerne lignin fra træ og erstatte det med en polymer. Kredit:WILEY‐VCH Verlag GmbH &Co. KGaA, Weinheim, licenseret under CC BY-NC-ND 4.0 Da Timothée Boitouzet stude
Gennemsigtigt træ:fremtidens byggemateriale?Gennemsigtigt træ skabes ved at fjerne lignin fra træ og erstatte det med en polymer. Kredit:WILEY‐VCH Verlag GmbH &Co. KGaA, Weinheim, licenseret under CC BY-NC-ND 4.0 Da Timothée Boitouzet stude
- Hvordan bruger et batteri til at tænde din lommelygte demonstrere overførsel af energi?
- Hvad spiser en Milkweed -plante?
- Hvad er navnene på nogle videnskabsværktøjer?
- Hvad er den kemiske formel for kobber II dihydrogenphosphat?
- Er NaF surt basisk eller et salt?
- Hvordan betragtes fysik som en livsstil?


