Hvordan oxideres en sammensat?
Her er en sammenbrud af processen:
Tab af elektroner:
* Oxidation involverer fjernelse af elektroner fra en forbindelse. Dette fører til en stigning i oxidationstilstanden for atom (er) inden for forbindelsen.
* F.eks. I reaktionen af jern med ilt til dannelse af jernoxid (rust):
* Fe (jern) mister elektroner for at blive Fe³⁺ (jernioner)
* Denne proces kaldes oxidation .
Gevinst af ilt:
* Oxygen er et meget elektronegativt element, hvilket betyder, at det tiltrækker elektroner.
* Når en forbindelse får iltatomer, har oxygenatomerne en tendens til at trække elektroner væk fra de andre atomer i forbindelsen, hvilket forårsager oxidation.
* F.eks. Ved forbrænding af metan (ch₄):
* Methan (CH₄) reagerer med ilt (O₂) for at danne kuldioxid (CO₂) og vand (H₂O).
* Carbonatomet i metan får ilt og bliver kuldioxid (CO₂).
* Denne proces kaldes også oxidation .
Nøglepunkter:
* Oxidation og reduktion sker altid sammen: Oxidation ledsages altid af en reduktionsreaktion, hvor et andet stof får elektroner eller mister ilt. Dette er kendt som en redox -reaktion .
* Oxidationstilstand: Oxidationstilstanden for et atom afspejler antallet af elektroner, det har opnået eller mistet.
* Oxidation er ikke altid en kemisk reaktion: Det kan også være en biologisk proces, såsom nedbrydning af glukose i kroppen for energi.
Eksempler på oxidation:
* forbrænding: Brændende brændstoffer som træ, propan og benzin.
* Korrosion: Rust af jern, pletter af sølv.
* respiration: Opdeling af mad i levende organismer.
Fortæl mig, hvis du gerne vil have mere specifikke eksempler eller have yderligere spørgsmål!
 Varme artikler
Varme artikler
-
 Forskere udvikler en ny metode til levering af glukagonSihan Yu og Matthew Webber. Kredit:University of Notre Dame For børn med type 1-diabetes, risikoen for at opleve en alvorlig hypoglykæmisk episode er særlig almindelig – og for forældre, truslen o
Forskere udvikler en ny metode til levering af glukagonSihan Yu og Matthew Webber. Kredit:University of Notre Dame For børn med type 1-diabetes, risikoen for at opleve en alvorlig hypoglykæmisk episode er særlig almindelig – og for forældre, truslen o -
 Skrubning af kuldioxid fra røgstokke til renere industrielle emissionerKredit:CC0 Public Domain Et internationalt team ledet af en kemiforsker ved Oregon State University har afdækket en bedre måde at skrubbe kuldioxid fra røgstøvemissioner, hvilket kan være en nøgle
Skrubning af kuldioxid fra røgstokke til renere industrielle emissionerKredit:CC0 Public Domain Et internationalt team ledet af en kemiforsker ved Oregon State University har afdækket en bedre måde at skrubbe kuldioxid fra røgstøvemissioner, hvilket kan være en nøgle -
 Probiotiske hydrogeler heler tarmsår, andre bandager ikke kan nåMikroskopisk billede af en bakteriel hydrogel, der binder til slimproteiner på overfladen af tarmvæggen. Kredit:Wyss Institute ved Harvard University Udvendige sår såsom hudsår eller hudafskrabn
Probiotiske hydrogeler heler tarmsår, andre bandager ikke kan nåMikroskopisk billede af en bakteriel hydrogel, der binder til slimproteiner på overfladen af tarmvæggen. Kredit:Wyss Institute ved Harvard University Udvendige sår såsom hudsår eller hudafskrabn -
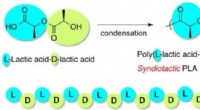 Fremgangsmåde til at syntetisere en ny polyester med alternerende arrangementFremgangsmåde til syntetisering af rene syndiotaktiske poly(mælkesyre)polyestere og billede af sfærulit deraf. Grafisk abstrakt af Polymerkemi , 2018, 9, 2446-2457. DOI:10.1039/C8PY00391B-Reproducer
Fremgangsmåde til at syntetisere en ny polyester med alternerende arrangementFremgangsmåde til syntetisering af rene syndiotaktiske poly(mælkesyre)polyestere og billede af sfærulit deraf. Grafisk abstrakt af Polymerkemi , 2018, 9, 2446-2457. DOI:10.1039/C8PY00391B-Reproducer
- Forskere arbejder på at forbedre genopretning fra tætte skiferreservoirer
- Afgørende for livet, havene får chancer i klimaspotlight
- Hackere frigiver data, efter at LA skoledistrikt nægter at betale løsesum
- Hvad afspejler energi fra solen i atmosfæren?
- Hvordan bruges videnskab i mekanik?
- Landformen, der bedst beskriver skove?


