Hvor mange molekyler af LICL er der i en 127,17 g prøve?
1. Find den molære masse af licl:
* Li (lithium) har en molmasse på 6,941 g/mol
* Cl (klor) har en molmasse på 35,453 g/mol
* Molmasse licl =6,941 g/mol + 35,453 g/mol =42,394 g/mol
2. Beregn antallet af mol licl:
* Mol =masse / molær masse
* Mol =127,17 g / 42,394 g / mol =3,00 mol
3. Brug Avogadros nummer for at finde antallet af molekyler:
* Avogadros nummer =6,022 x 10^23 molekyler/mol
* Antal molekyler =mol * Avogadro's nummer
* Antal molekyler =3,00 mol * 6,022 x 10^23 molekyler/mol =1,81 x 10^24 molekyler
Derfor er der ca. 1,81 x 10^24 molekyler licl i en 127,17 g prøve.
 Varme artikler
Varme artikler
-
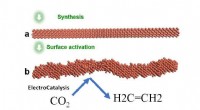 Forskere opdager en effektiv vej til at omdanne kuldioxid til ethylenIllustration af ElectroCatalysis-systemet, som syntetiserede den glatte nanotråd og derefter aktiverede den ved at påføre en spænding for at få den ru trinflade, der er meget selektiv for CO2-reduktio
Forskere opdager en effektiv vej til at omdanne kuldioxid til ethylenIllustration af ElectroCatalysis-systemet, som syntetiserede den glatte nanotråd og derefter aktiverede den ved at påføre en spænding for at få den ru trinflade, der er meget selektiv for CO2-reduktio -
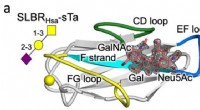 Udnyttelse af strukturen af bakterielle værtscellereceptorer til at påvise cancerKrystalstruktur af en streptococcus SLBR (Hsa) binding med høj affinitet til værtscellens glycanreceptor (sTa). Variation i sekvens og struktur af de mærkede SLBR-proteinsløjfer (CD, EF og FG) forudsi
Udnyttelse af strukturen af bakterielle værtscellereceptorer til at påvise cancerKrystalstruktur af en streptococcus SLBR (Hsa) binding med høj affinitet til værtscellens glycanreceptor (sTa). Variation i sekvens og struktur af de mærkede SLBR-proteinsløjfer (CD, EF og FG) forudsi -
 Nye resultater muliggør overvågning for skadelige toksiner i ferskvandsmiljøerMikroskopbillede af den guanitoksin-producerende cyanobakterie Sphaerospermopsis torques-reginae. Kredit:Vera Regina Werner Et internationalt hold af forskere har identificeret de gener og den bios
Nye resultater muliggør overvågning for skadelige toksiner i ferskvandsmiljøerMikroskopbillede af den guanitoksin-producerende cyanobakterie Sphaerospermopsis torques-reginae. Kredit:Vera Regina Werner Et internationalt hold af forskere har identificeret de gener og den bios -
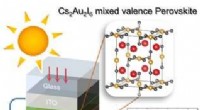 Blyfri, effektiv perovskit til fotovoltaiske cellerFigur 1. Skematisk over struktur af fuld solcelleenhed. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Et forskerhold fra KAIST har foreslået et perovskitmateriale, Cs 2 Au 2
Blyfri, effektiv perovskit til fotovoltaiske cellerFigur 1. Skematisk over struktur af fuld solcelleenhed. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Et forskerhold fra KAIST har foreslået et perovskitmateriale, Cs 2 Au 2
- Hvad er en luftballon drevet af?
- Router-kompromis, useriøs fjernbetjening? Nemt, siger ISE
- Ny indsigt i A-vitamin genbrug og dagtidssyn
- Hvad er alle grene og underfalter?
- Hvordan påvirker den afstand, gennem hvilken kraft anvendes, arbejdet?
- Ny metode til billeddannelse af udåndet åndedrag kan give indsigt i COVID-19-transmission


