Ammoniumphosphat plus bariumhydroxid - hydroxid?
Her er den afbalancerede kemiske ligning:
2 (nh₄) ₃po₄ (aq) + 3ba (OH) ₂ (aq) → ba₃ (po₄) ₂ (s) + 6nh₄oh (aq)
Forklaring:
* ammoniumphosphat ((NH₄) ₃po₄) er en opløselig ionisk forbindelse.
* bariumhydroxid (BA (OH) ₂) er også en opløselig ionisk forbindelse.
* bariumphosphat (ba₃ (po₄) ₂) er en uopløselig ionisk forbindelse, hvilket betyder, at den vil udfælde ud af opløsningen som et fast stof.
* ammoniumhydroxid (NH₄OH) er en svag base, der findes i ligevægt med ammoniak (NH₃) og vand (H₂O).
Nøgleobservationer:
* Et hvidt bundfald af bariumphosphat dannes.
* Opløsningen bliver lidt grundlæggende på grund af dannelsen af ammoniumhydroxid.
Bemærk: Ammoniumhydroxid er ofte skrevet som NH₄OH, men det er vigtigt at huske, at det findes i ligevægt med ammoniak og vand:
nh₄oh (aq) ⇌ nh₃ (aq) + h₂o (l)
 Varme artikler
Varme artikler
-
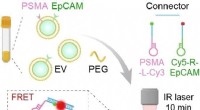 Hurtig, ukompliceret og specifik:Diagnose af prostatacancer fra blodprøverGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202207037 Tidlig opdagelse af prostatacancer, en af de mest almindelige kræftformer hos mænd, opnås ofte
Hurtig, ukompliceret og specifik:Diagnose af prostatacancer fra blodprøverGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202207037 Tidlig opdagelse af prostatacancer, en af de mest almindelige kræftformer hos mænd, opnås ofte -
 Syntetisk gummi overgår naturgummiIndledende test af dæk fremstillet af de naturidentiske, biomimetisk syntetisk gummi BISYKA viser, at de opnår omkring 30 til 50 procent mindre slid i forhold til naturgummidæk. Kredit:Fraunhofer IAP/
Syntetisk gummi overgår naturgummiIndledende test af dæk fremstillet af de naturidentiske, biomimetisk syntetisk gummi BISYKA viser, at de opnår omkring 30 til 50 procent mindre slid i forhold til naturgummidæk. Kredit:Fraunhofer IAP/ -
 Video:Hvordan måler vi temperatur?Kredit:The American Chemical Society Vi har stor tillid til, at vi måler temperaturen nøjagtigt. Men hvordan fungerer termometre i køkkenet eller på lægekontoret? Takket være termodynamikkens love
Video:Hvordan måler vi temperatur?Kredit:The American Chemical Society Vi har stor tillid til, at vi måler temperaturen nøjagtigt. Men hvordan fungerer termometre i køkkenet eller på lægekontoret? Takket være termodynamikkens love -
 Vi komposterede bionedbrydelige balloner. Her er hvad vi fandt efter 16 ugerBionedbrydelige balloner efter 16 uger i ferskvand. Kredit:Jesse Benjamin, Forfatter angivet Efter 16 uger i en industriel kompostbunke, vi udgravede blå og hvide balloner og fandt dem helt uskadt
Vi komposterede bionedbrydelige balloner. Her er hvad vi fandt efter 16 ugerBionedbrydelige balloner efter 16 uger i ferskvand. Kredit:Jesse Benjamin, Forfatter angivet Efter 16 uger i en industriel kompostbunke, vi udgravede blå og hvide balloner og fandt dem helt uskadt


