Hvorfor er calciumoxid en ionisk binding?
* Elektronegativitet: Elektronegativitet er et atomens tendens til at tiltrække elektroner mod sig selv i en kemisk binding. Oxygen er meget elektronegativ, mens calcium er meget mindre elektronegativ. Denne forskel i elektronegativitet er afgørende for ionisk binding.
* Elektronoverførsel: Når calcium og ilt reagerer, "stjæler det stærkt elektronegative iltatom fuldstændigt" et elektron fra calciumatomet. Dette resulterer i:
* Calcium (CA) mister to elektroner og bliver en positivt ladet ion (Ca²⁺).
* Oxygen (O) At få to elektroner og blive en negativt ladet ion (O²⁻).
* Elektrostatisk attraktion: De modsatte ladede ioner (Ca²⁺ og O²⁻) tiltrækkes derefter af hinanden af stærke elektrostatiske kræfter, der danner det ioniske forbindelsescalciumoxid.
nøglefunktioner ved ioniske bindinger:
* overførsel af elektroner: Det ene atom mister elektroner fuldstændigt, og det andet atom får disse elektroner.
* Dannelse af ioner: Elektronoverførslen fører til dannelse af modsat ladede ioner.
* Elektrostatisk attraktion: De modsatte ladede ioner holdes sammen af stærke elektrostatiske kræfter og danner den ioniske binding.
Sammenfattende driver den store forskel i elektronegativitet mellem calcium og ilt overførslen af elektroner, hvilket fører til dannelsen af ioner og den stærke elektrostatiske tiltrækning, der kendetegner den ioniske binding i calciumoxid.
Sidste artikelHvad er den kemiske formel for kviksølv I -fosfat?
Næste artikelHvad er reaktionen ved at tilsætte jernoxid til en syre?
 Varme artikler
Varme artikler
-
 Defekt kulstof forenkler produktionen af brintoverilteForskere ved Rice University har introduceret plasmabehandlet kønrøg som en enkel og yderst effektiv katalysator til produktion af hydrogenperoxid. Defekter skabt i kulstoffet giver flere katalytiske
Defekt kulstof forenkler produktionen af brintoverilteForskere ved Rice University har introduceret plasmabehandlet kønrøg som en enkel og yderst effektiv katalysator til produktion af hydrogenperoxid. Defekter skabt i kulstoffet giver flere katalytiske -
 Forskere har opdaget, hvordan blodorme fremstiller deres unikke kobbertænderVenstre:Billede af den udbøjede snabel af Glycera dibranchiata med dens fire fritlagte kæber, højre:Scanningselektronmikroskopbillede af en Glycera-kæbe (Skalastang, 0,5 mm). Kredit:Matter/Wonderly et
Forskere har opdaget, hvordan blodorme fremstiller deres unikke kobbertænderVenstre:Billede af den udbøjede snabel af Glycera dibranchiata med dens fire fritlagte kæber, højre:Scanningselektronmikroskopbillede af en Glycera-kæbe (Skalastang, 0,5 mm). Kredit:Matter/Wonderly et -
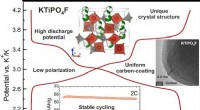 Forskere udvikler et nyt katodemateriale til metal-ion-batterierForskere fra Skoltech Center for Energy Science and Technology (CEST) skabte et nyt katodemateriale baseret på titaniumfluoridfosfat, hvilket muliggjorde opnåelse af overlegen energiydelse og stabil d
Forskere udvikler et nyt katodemateriale til metal-ion-batterierForskere fra Skoltech Center for Energy Science and Technology (CEST) skabte et nyt katodemateriale baseret på titaniumfluoridfosfat, hvilket muliggjorde opnåelse af overlegen energiydelse og stabil d -
 Forskere finder, at 2-D overgangsmetalkarbider reagerer med vand, åbner en dør til deres ukendte k…MXenes reaktivitet over for vand er vist i dette eksperiment, hvor en Ti-carbid MXene overlever længere i en iltmættet, ikke-vandigt system, i modsætning til det samme MXene dispergeret i argon-mættet
Forskere finder, at 2-D overgangsmetalkarbider reagerer med vand, åbner en dør til deres ukendte k…MXenes reaktivitet over for vand er vist i dette eksperiment, hvor en Ti-carbid MXene overlever længere i en iltmættet, ikke-vandigt system, i modsætning til det samme MXene dispergeret i argon-mættet
- Hvad kan stjerner af et binært system gøre?
- Svigtende iskældre signalerer ændringer i Alaskas hvalfangstbyer
- Betyder acceleration at fremskynde og bremse?
- Moderne vulkanisme knyttet til begivenheder, der indtræffer kort efter Jordens fødsel
- Deep learning kombinerer fordelene ved holografi og lysfeltsmikroskopi til 3-D-billeddannelse
- Aerogeler til solcelleanlæg og vinduer


