Hvad er reaktionen ved at tilsætte jernoxid til en syre?
1. Jern (II) Oxid (Feo) med syre:
* reaktion: Feo + 2H⁺ → Fe²⁺ + H₂O
* Beskrivelse: Jern (II) oxid reagerer med syrer for at danne jern (II) -ioner (Fe²⁺) og vand.
* Eksempel: Feo + 2HCl → Fecl₂ + H₂O
2. Jern (III) Oxid (Fe₂o₃) med syre:
* reaktion: Fe₂o₃ + 6H⁺ → 2Fe³⁺ + 3H₂O
* Beskrivelse: Jern (III) oxid reagerer med syrer for at danne jern (III) ioner (Fe³⁺) og vand.
* Eksempel: Fe₂o₃ + 6HNO₃ → 2FE (NO₃) ₃ + 3H₂O
3. Jern (II, III) Oxid (Fe₃o₄) med syre:
* reaktion: Fe₃o₄ + 8H⁺ → 2Fe³⁺ + Fe²⁺ + 4H₂O
* Beskrivelse: Jern (II, III) oxid, også kendt som magnetit, reagerer med syrer for at danne både jern (II) og jern (III) -ioner sammen med vand.
* Eksempel: Fe₃o₄ + 8HCl → 2Fecl₃ + fecl₂ + 4H₂O
Vigtige noter:
* Syrestyrke: Reaktionshastigheden og omfanget af reaktionen afhænger af styrken af den anvendte syre. Stærkere syrer som saltsyre (HCI) og salpetersyre (HNO₃) reagerer lettere og fuldstændigt.
* Dannelse af salte: Reaktionen mellem jernoxider og syrer danner generelt jernsalte. Den specifikke salt dannet afhænger af den anvendte syre (f.eks. Fecl₂ med HCI, Fe (NO₃) ₃ med HNO₃).
* Oxidationstilstand: Oxidationstilstanden for jern i jernoxid bestemmer oxidationstilstanden for jern i det resulterende salt.
* Varmeproduktion: Reaktionen er ofte eksoterm, hvilket betyder, at den frigiver varme.
Kortfattet:
Reaktionen af jernoxid med en syre resulterer i dannelsen af jernioner og vand. Den specifikke type jernoxid og den anvendte syre bestemmer de nøjagtige produkter og reaktionsbetingelser.
Sidste artikelHvorfor er calciumoxid en ionisk binding?
Næste artikelHvad er reaktionen af arsen og jern III -hydroxid?
 Varme artikler
Varme artikler
-
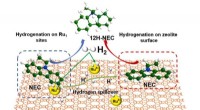 Synergistiske katalysatorer til højeffektiv brintlagringGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121958 Brintenergi betragtes som lovende vedvarende energi. Udviklingen af brintenergi er imidlertid begrænset
Synergistiske katalysatorer til højeffektiv brintlagringGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121958 Brintenergi betragtes som lovende vedvarende energi. Udviklingen af brintenergi er imidlertid begrænset -
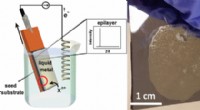 En billigere, grønnere måde at dyrke krystallinske halvlederfilm påKredit:ACS University of Michigan kemikere har udviklet en grønnere, billigere måde at lave enkeltkrystallinske halvlederfilm på, komponenter i hjertet af alle vores elektriske gadgets. Enkeltkry
En billigere, grønnere måde at dyrke krystallinske halvlederfilm påKredit:ACS University of Michigan kemikere har udviklet en grønnere, billigere måde at lave enkeltkrystallinske halvlederfilm på, komponenter i hjertet af alle vores elektriske gadgets. Enkeltkry -
 En mere sikker måde at fremstille azider til brug i klikkemien, Syntese af FSO2N3. Reaktionsbetingelser:1 (7,9 g, 24 mmol), NaN3 (1,3 g, 20 mmol), MTBE/MeCN/H2O (84 ml, 10:1:10, v/v/v), 0 °C, luft, 10 min. b, Diazotransferreaktion mellem amlodipin (2a) og FSO2
En mere sikker måde at fremstille azider til brug i klikkemien, Syntese af FSO2N3. Reaktionsbetingelser:1 (7,9 g, 24 mmol), NaN3 (1,3 g, 20 mmol), MTBE/MeCN/H2O (84 ml, 10:1:10, v/v/v), 0 °C, luft, 10 min. b, Diazotransferreaktion mellem amlodipin (2a) og FSO2 -
 Olivenmøllens spildevand omdannet:Fra forurenende stof til biogødning, biobrændstofKredit:American Chemical Society Olivenolie har længe været et populært køkkenprodukt. Men produktionen af olien skaber en stor strøm af spildevand, der kan forurene vandveje, reducere jordens f
Olivenmøllens spildevand omdannet:Fra forurenende stof til biogødning, biobrændstofKredit:American Chemical Society Olivenolie har længe været et populært køkkenprodukt. Men produktionen af olien skaber en stor strøm af spildevand, der kan forurene vandveje, reducere jordens f
- Hvorfor var det ikke så langt side af månen var ukendt indtil 1959?
- Hvad er brugen af dummy wire?
- Hvorfor er der kun love for gasser og ikke faste stoffer eller væsker?
- Kinas rumlaboratorium kan falde til Jorden senere:European Space Agency
- Falder vandmassen, når salt tilsættes?
- Hvor får folk deres energi fra?


