Hvad er en ion-dipolbinding?
Her er en sammenbrud:
1. Ioner: Dette er atomer eller grupper af atomer, der har opnået eller mistet elektroner, hvilket resulterer i en nettopositiv eller negativ ladning.
2. Polære molekyler: Disse molekyler har en permanent ujævn fordeling af elektrondensitet, hvilket skaber en positiv og negativ ende (en "dipol"). Tænk på vand (H₂O) med dets iltatom med en lidt negativ ladning og brintatomerne har en lidt positiv ladning.
3. Interaktionen: Den positive ende af det polære molekyle tiltrækkes af den negative ion, og vice versa. Denne attraktion opstår fra de elektrostatiske kræfter mellem modsatte afgifter.
Nøglefunktioner:
* styrke: Ion-dipolbindinger er generelt stærkere end van der Waals-kræfter, men svagere end hydrogenbindinger eller ioniske bindinger. Styrken afhænger af ladningen af ion og størrelsen af dipolmomentet for det polære molekyle.
* Retning: Interaktionen er retningsbestemt, hvilket betyder, at ion og det polære molekyle er nødt til at tilpasse sig hinanden for maksimal tiltrækning.
* Betydning: Ion-dipolinteraktioner spiller en afgørende rolle i opløsning af ioniske forbindelser i polære opløsningsmidler som vand. De bidrager også til egenskaberne ved mange biologiske systemer, som interaktion mellem ioner og proteiner.
Eksempler:
* salt (NaCl) opløste i vand: De positive natriumioner (Na+) tiltrækkes af den negative ende af vandmolekyler (ilt), mens de negative chloridioner (Cl-) tiltrækkes af den positive ende af vandmolekyler (hydrogen). Denne interaktion hjælper med at bryde saltet ionisk gitter og giver den mulighed for at opløses.
* Hydrering af ioner i opløsning: Ioner i opløsning er omgivet af en skal af polære opløsningsmiddelmolekyler, der tiltrækkes af ionens ladning gennem ion-dipol-interaktioner.
Sammenfattende er en ion-dipolbinding en elektrostatisk attraktion mellem en ladet ion og et polært molekyle. Det spiller en afgørende rolle i forskellige kemiske og biologiske processer, der påvirker opløseligheden af ioniske forbindelser, hydrering af ioner og interaktioner mellem biomolekyler.
 Varme artikler
Varme artikler
-
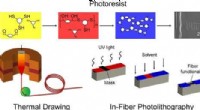 Mønstermetode kunne bane vejen for nye fiberbaserede enheder, smarte tekstilerKredit:American Chemical Society Multimateriale fibre, der integrerer metal, glas og halvledere kan være nyttige til anvendelser som biomedicin, smarte tekstiler og robotter. Men fordi fibrene er
Mønstermetode kunne bane vejen for nye fiberbaserede enheder, smarte tekstilerKredit:American Chemical Society Multimateriale fibre, der integrerer metal, glas og halvledere kan være nyttige til anvendelser som biomedicin, smarte tekstiler og robotter. Men fordi fibrene er -
 Enkeltcelleanalyse afslører heterogenitet i metaladsorptionKredit:LuckyStep/Shutterstock Biosorption er fjernelse af kontaminanter fra en prøve ved at adsorbere dem på overfladen af et biologisk materiale. Det forventes at give miljømæssige og økonomiske
Enkeltcelleanalyse afslører heterogenitet i metaladsorptionKredit:LuckyStep/Shutterstock Biosorption er fjernelse af kontaminanter fra en prøve ved at adsorbere dem på overfladen af et biologisk materiale. Det forventes at give miljømæssige og økonomiske -
 Registrering af skadelige molekyler med lysLysbølger, der bevæger sig på isolerende eller dielektriske materialer, såsom glas, kan øge følsomheden for optiske sensorer og kan være tilgængelige kommercielt inden for få år. Kredit:andreadonetti
Registrering af skadelige molekyler med lysLysbølger, der bevæger sig på isolerende eller dielektriske materialer, såsom glas, kan øge følsomheden for optiske sensorer og kan være tilgængelige kommercielt inden for få år. Kredit:andreadonetti -
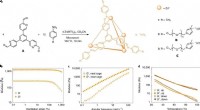 Porøs væske rummer større molekylerForberedelse og reologi af bure 1-3. Kredit: Naturkemi (2020). DOI:10.1038/s41557-020-0419-2 Et internationalt team af kemikere har udviklet en metode til at skabe en ionisk væske, porøs, tetraed
Porøs væske rummer større molekylerForberedelse og reologi af bure 1-3. Kredit: Naturkemi (2020). DOI:10.1038/s41557-020-0419-2 Et internationalt team af kemikere har udviklet en metode til at skabe en ionisk væske, porøs, tetraed


