Hvilket volumen ml af en koncentreret opløsning natriumhydroxid 6,00 m skal fortyndes til 200,0 gøre 0,880 hydroxid?
forståelse af koncepterne
* Molaritet (M): Repræsenterer koncentrationen af en opløsning, udtrykt som mol af opløst stof pr. Liter opløsning.
* fortynding: Processen med at reducere koncentrationen af en opløsning ved at tilsætte mere opløsningsmiddel.
* fortynding ligning: M₁v₁ =m₂v₂
* M₁ =molaritet af den koncentrerede opløsning
* V₁ =volumen af den koncentrerede løsning
* M₂ =molaritet af den fortyndede opløsning
* V₂ =volumen af den fortyndede opløsning
Beregninger
1. Identificer de kendte værdier:
* M₁ =6,00 m (koncentration af koncentreret NaOH)
* M₂ =0,880 m (ønsket koncentration af fortyndet NaOH)
* V₂ =200,0 ml (slutvolumen af den fortyndede opløsning)
2. Tilslut værdierne i fortyndingsligningen:
* (6,00 m) * V₁ =(0,880 m) * (200,0 ml)
3. Løs for V₁ (mængden af koncentreret NaOH):
* V₁ =[(0,880 m) * (200,0 ml)] / (6,00 m)
* V₁ =29,3 ml
Svar:
Du skal fortynde 29,3 ml af den 6,00 m natriumhydroxidopløsning til at fremstille 200,0 ml af en 0,880 m opløsning.
 Varme artikler
Varme artikler
-
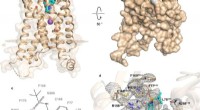 Undersøgelse afslører strukturen af receptor impliceret i type 2 -diabetes og mereFig. 1:Struktur og bindingssted for hBLT1. Kredit:Michaelian, N., et al. Naturkommunikation , https://doi.org/10.1038/s41467-021-23149-1 Forskere fra University of Southern California, Merck &Co
Undersøgelse afslører strukturen af receptor impliceret i type 2 -diabetes og mereFig. 1:Struktur og bindingssted for hBLT1. Kredit:Michaelian, N., et al. Naturkommunikation , https://doi.org/10.1038/s41467-021-23149-1 Forskere fra University of Southern California, Merck &Co -
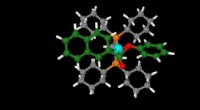 Enkel bytte til et grønnere værktøjskasseEn bidentat ligand (orange og grå) på nikkelatomet (blå) fremmer eliminering af carbonyl i esteren (grøn og rød) i denne overgangstilstand. Kredit:KAUST En metalkatalysator, der giver tydelige car
Enkel bytte til et grønnere værktøjskasseEn bidentat ligand (orange og grå) på nikkelatomet (blå) fremmer eliminering af carbonyl i esteren (grøn og rød) i denne overgangstilstand. Kredit:KAUST En metalkatalysator, der giver tydelige car -
 Naturinspireret krystalstruktur forudsigelseForskere fra Rusland fandt en måde at forbedre forudsigelsesalgoritmerne for krystalstruktur, gør opdagelsen af nye forbindelser flere gange hurtigere. Kredit:MIPT Forskere fra Rusland har rappo
Naturinspireret krystalstruktur forudsigelseForskere fra Rusland fandt en måde at forbedre forudsigelsesalgoritmerne for krystalstruktur, gør opdagelsen af nye forbindelser flere gange hurtigere. Kredit:MIPT Forskere fra Rusland har rappo -
 En måde at reparere tandemalje påSnapshot af reparationseksperimentet på en menneskelig tand. Kredit:Zhejiang University Et team af forskere fra Zhejiang University og Xiamen University har fundet en måde at reparere menneskelig
En måde at reparere tandemalje påSnapshot af reparationseksperimentet på en menneskelig tand. Kredit:Zhejiang University Et team af forskere fra Zhejiang University og Xiamen University har fundet en måde at reparere menneskelig
- Todimensionel MXene som et nyt elektrodemateriale til næste generations display
- Kinesisk rumlaboratorium falder tilbage til Jorden i marts
- Hvad er virkningerne af forvitring på sten?
- Når en organisme vokser den skaber sag og derfor modbeviser loven om bevaringsenergi?
- Er CCl4 en ionisk eller molekylær forbindelse?
- Type biologisk middel, der handler for at skelne mellem en organisme ved at overvælde den evne, der…


