Hvorfor skal ammoniak tørres inden en reaktion med natrium?
1. Sikkerhedsmæssige bekymringer:
* natrium er et meget reaktivt metal: Det reagerer voldsomt med vand og genererer brintgas, som er brandfarlig og eksplosiv. Selv spor af vand i ammoniak kan udløse denne reaktion.
* Dannelse af natriumhydroxid: Vand reagerer med natrium til dannelse af natriumhydroxid (NaOH), som er en stærk base og kan yderligere komplicere reaktionen.
2. Reaktionsspecificitet:
* ønsket reaktion: Den ønskede reaktion mellem natrium og ammoniak er dannelsen af natriumamid (NANH2), en stærk base anvendt i organisk syntese.
* Konkurrerende reaktion: Vand konkurrerer med ammoniak om reaktion med natrium. Dette fører til en blanding af produkter, herunder natriumhydroxid og natriumamid, hvilket kan påvirke udbyttet og renheden af det ønskede produkt.
3. Reaktionseffektivitet:
* vand som hæmmer: Vand kan fungere som en hæmmer i reaktionen mellem natrium og ammoniak. Det kan bremse reaktionshastigheden og mindske den samlede effektivitet af processen.
Metoder til tørring af ammoniak:
* tørringsmidler: Almindelige tørringsmidler, der anvendes til ammoniak, inkluderer natriummetal, calciumoxid og kaliumhydroxid. Disse midler absorberer let vand fra ammoniakgassen.
* destillation: Ammoniak kan tørres ved destillation. Dette involverer opvarmning af ammoniakgas og opsamling af den tørrede gas i en separat beholder.
Som konklusion er tørring af ammoniak afgørende for at sikre en sikker, kontrolleret og effektiv reaktion med natrium. Det forhindrer dannelse af uønskede biprodukter, maksimerer udbyttet af natriumamid og minimerer sikkerhedsrisici.
Sidste artikelHvad sker der, når vandmiljøer bliver sure?
Næste artikelWhat is nitrogen hydrogen oxygen beryllium flouride?
 Varme artikler
Varme artikler
-
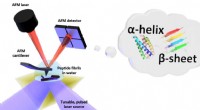 Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s
Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s -
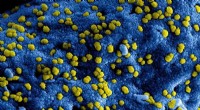 Ny bakterietestmetode til at forbedre sundhedsplejen, fødevaresikkerhed og meget mereKredit:Unsplash/CC0 Public Domain Påvisning af levedygtige bakterier er vigtigt for forskellige områder, fra fødevaresikkerhed til medicinsk diagnose. De eksisterende teknikker til at udføre antib
Ny bakterietestmetode til at forbedre sundhedsplejen, fødevaresikkerhed og meget mereKredit:Unsplash/CC0 Public Domain Påvisning af levedygtige bakterier er vigtigt for forskellige områder, fra fødevaresikkerhed til medicinsk diagnose. De eksisterende teknikker til at udføre antib -
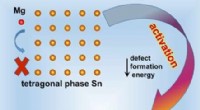 Fasegrænseregulering, der øger den elektrokemiske reaktivitet af tinbaserede anoder til magnesium-…Ved at introducere den anden fase gør den øgede fasegrænse Mg lettere at diffundere og indgå i Sn, hvilket effektivt stimulerer den elektrokemiske reaktivitet af Sn med Mg. Kredit:Science China Press
Fasegrænseregulering, der øger den elektrokemiske reaktivitet af tinbaserede anoder til magnesium-…Ved at introducere den anden fase gør den øgede fasegrænse Mg lettere at diffundere og indgå i Sn, hvilket effektivt stimulerer den elektrokemiske reaktivitet af Sn med Mg. Kredit:Science China Press -
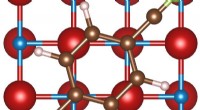 Solid-ion ledere for sikrere batterierInden for elektrokemi, det dendrit-undertrykkende domæne var endnu ikke blevet udforsket, selvom det dendrit-blokerende regime allerede var velkendt og undersøgt. Kredit:College of Engineering, Carneg
Solid-ion ledere for sikrere batterierInden for elektrokemi, det dendrit-undertrykkende domæne var endnu ikke blevet udforsket, selvom det dendrit-blokerende regime allerede var velkendt og undersøgt. Kredit:College of Engineering, Carneg
- Hvad er navnene på stjerner større end sol?
- Kan to planeter kredse hinanden?
- Undersøgelse finder ud af, at du får, hvad du betaler for, med online Q &A-sider
- Antigenspecifik målretning af immunsystemet tilbyder behandlingstilgang til forbedring af biologisk…
- Hvordan beviste Isaac Newton, at solen er centrum af universet?
- Eventyr i faserum:Forenet kort på plastik og elastiske glas


