Hvad kombineres let med brintioner?
Her er en sammenbrud:
* baser indeholder hydroxidioner (OH-), der let reagerer med brintioner for at danne vand. Dette er det grundlæggende grundlag for syre-base-neutralisering.
* Alkaliske stoffer ligner baser, men indeholder muligvis ikke hydroxidioner direkte. De kan stadig reagere med brintioner for at producere vand og et salt.
Eksempel:
* saltsyre (HCL) er en stærk syre, hvilket betyder, at den let frigiver hydrogenioner. Når det reagerer med natriumhydroxid (NaOH) , en stærk base, den danner vand (H2O) og natriumchlorid (NaCl) - salt :
`` `
HCL (aq) + NaOH (aq) → H2O (l) + NaCl (aq)
`` `
Kortfattet:
* baser og alkaliske stoffer er de mest almindelige stoffer, der let kombineres med brintioner.
* Denne reaktion er et grundlæggende koncept inden for kemi kendt som syre-base neutralisering .
* Produktet af denne reaktion er altid vand og et salt .
 Varme artikler
Varme artikler
-
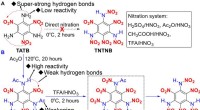 Syntese af TNTNB repræsenterer ny energitop for organiske sprængstofferSyntese af TNTNB.(A) Mislykket nitrering fra TATB til TNTNB ved brug af forskellige nitreringssystemer. (B) Syntese af TNTNB under anvendelse af den foreslåede acylerings-aktiverings-nitreringsstrateg
Syntese af TNTNB repræsenterer ny energitop for organiske sprængstofferSyntese af TNTNB.(A) Mislykket nitrering fra TATB til TNTNB ved brug af forskellige nitreringssystemer. (B) Syntese af TNTNB under anvendelse af den foreslåede acylerings-aktiverings-nitreringsstrateg -
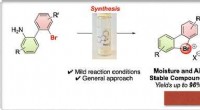 Cykliske hypervalente brom virker som aryne forstadierKredit:Wiley Diaryl λ 3 -bromaner er en sjælden og generelt uforsket klasse af forbindelser. En mild og effektiv protokol leverer nu en bred palet af disse interessante byggesten til organisk sy
Cykliske hypervalente brom virker som aryne forstadierKredit:Wiley Diaryl λ 3 -bromaner er en sjælden og generelt uforsket klasse af forbindelser. En mild og effektiv protokol leverer nu en bred palet af disse interessante byggesten til organisk sy -
 Hvordan edderkoppesilke en dag kunne bruges i kræftbehandlingKredit:Vadym Lesyk/Shutterstock Kræft er samtidig en af de mest almindelige og ødelæggende sygdomme i vores samfund. Så at finde nye måder at behandle det på er en vedvarende videnskabelig udford
Hvordan edderkoppesilke en dag kunne bruges i kræftbehandlingKredit:Vadym Lesyk/Shutterstock Kræft er samtidig en af de mest almindelige og ødelæggende sygdomme i vores samfund. Så at finde nye måder at behandle det på er en vedvarende videnskabelig udford -
 Forskere udvikler materialer, der kan revolutionere, hvordan lys udnyttes til solenergiMagnetfeltdata, der viser dannelsen og forfaldet af excitonerne genereret af singlet fission. Kredit:A. Asadpoor Darvish, McCamey Lab Forskere ved Columbia University har udviklet en måde at udn
Forskere udvikler materialer, der kan revolutionere, hvordan lys udnyttes til solenergiMagnetfeltdata, der viser dannelsen og forfaldet af excitonerne genereret af singlet fission. Kredit:A. Asadpoor Darvish, McCamey Lab Forskere ved Columbia University har udviklet en måde at udn
- Er livet for én procent mindre overdådigt, end vi tror?
- Hvorfor bliver nogle tilfælde af seksuel forseelse urapporteret? Det er kompliceret
- Hvilket lag er den koldeste region i?
- Deep Neural Network har til formål at forbedre billeddannelse af celler
- Er vand en fossil brændstofenergi?
- WHOI undervandsrobot tager den første kendte automatiserede prøve fra havet


