Hvordan fremstiller du 6N ammoniumhydroxid fra 30 procent opløsning?
forståelse af udtrykkene
* 6n: Dette henviser til en 6 normal løsning. Normalitet (n) er et mål for koncentration, der vedrører antallet af ækvivalenter af et stof pr. Liter opløsning. I tilfælde af ammoniumhydroxid (NH₄OH) svarer normaliteten til molariteten (M), fordi hvert molekyle af NH₄OH tilvejebringer en hydroxidion (OH⁻).
* 30% løsning: Dette henviser til en opløsning, der er 30% ammoniumhydroxid efter vægt.
Beregninger
1. Bestem molariteten af 30% -opløsningen:
* Du har brug for densiteten af den 30% ammoniumhydroxidopløsning. Denne værdi kan variere lidt afhængigt af kilden, men en almindelig værdi er ca. 0,88 g/ml.
* Beregn massen af NH₄OH i 100 ml opløsning:
* Masse =volumen x densitet =100 ml x 0,88 g/ml =88 g
* Massen af NH₄OH =0,30 x 88 g =26,4 g
* Konverter masse af NH₄OH til mol:
* Mol =masse / molmasse =26,4 g / 17,03 g / mol =1,55 mol
* Beregn molariteten (M):
* Molaritet =mol / volumen (i liter) =1,55 mol / 0,1 l =15,5 m
2. Beregn fortyndingsfaktoren:
* Du vil have en 6n (eller 6m) løsning.
* Fortyndingsfaktor =indledende molaritet / endelig molaritet =15,5 m / 6 m =2,58
3. Forbered løsningen:
* Brug en volumetrisk kolbe: Vælg en volumetrisk kolbe med et volumen, der passer til den mængde opløsning, du har brug for (f.eks. 100 ml, 250 ml).
* Tilføj en lille mængde vand: Fyld kolben omtrent halvvejs med destilleret vand.
* Tilsæt omhyggeligt det koncentrerede ammoniumhydroxid: Ved hjælp af en gradueret cylinder tilsættes langsomt den 30% ammoniumhydroxidopløsning til kolben. Gør dette med forsigtighed, da varme kan genereres.
* top op med vand: Tilsæt den destillerede vand forsigtigt til kolben, indtil opløsningen når kalibreringsmærket på kolbenens hals.
* Bland grundigt: Stopper kolben og bland opløsningen grundigt ved at invertere den flere gange.
Sikkerhedsforholdsregler
* Bær passende sikkerhedsudstyr: Bær handsker, en laboratoriefrakke og beskyttelsesbriller for at beskytte dig selv mod kontakt med løsningen.
* arbejde i et godt ventileret område: Ammoniumhydroxid -dampe er irriterende og kan være giftige.
* Brug forsigtighed Ved håndtering af koncentrerede løsninger: Tilsæt altid syre til vand, aldrig vand til syre. Vær især forsigtig, når du arbejder med koncentreret ammoniak.
* Butik korrekt: Opbevar den forberedte opløsning i en tæt forseglet beholder i et køligt, tørt og godt ventileret område.
Vigtige noter:
* Nøjagtighed: Densiteten og koncentrationen af den 30% ammoniumhydroxidopløsning kan variere, så du kan være nødt til at justere dine beregninger i overensstemmelse hermed.
* fortynding: Du kan justere fortyndingsfaktoren for at fremstille løsninger af forskellige normaliteter.
Fortæl mig, hvis du har andre spørgsmål!
Sidste artikelHvorfor bruges ikke natriumhydroxid som en syre kur?
Næste artikelHvad er oxidationstilstanden for Mg i MGOH2?
 Varme artikler
Varme artikler
-
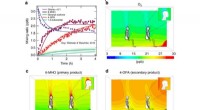 Pig-Pen-effekt:Blanding af hudolie og ozon kan producere en personlig forureningsskyNår ozon rammer olier på huden og i snavset tøj, det kan producere en personlig sky af irriterende stoffer. Kredit:Penn State Når ozon og hudolier mødes, den resulterende reaktion kan hjælpe med a
Pig-Pen-effekt:Blanding af hudolie og ozon kan producere en personlig forureningsskyNår ozon rammer olier på huden og i snavset tøj, det kan producere en personlig sky af irriterende stoffer. Kredit:Penn State Når ozon og hudolier mødes, den resulterende reaktion kan hjælpe med a -
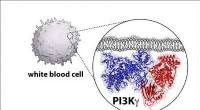 Kemikere udvikler en ny plan for enzym involveret i kræftKredit:University of Oregon Forskere har i årtier vidst, at en bestemt klasse af enzymer er en vigtig aktør inden for cellebiologi, fordi de ofte muterer og bliver væsentlige årsager til kræft. B
Kemikere udvikler en ny plan for enzym involveret i kræftKredit:University of Oregon Forskere har i årtier vidst, at en bestemt klasse af enzymer er en vigtig aktør inden for cellebiologi, fordi de ofte muterer og bliver væsentlige årsager til kræft. B -
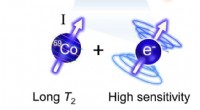 Kemikere designer kemisk sonde til at registrere små temperaturændringer i kroppenKredit:Colorado State University Den ikke-invasive, livreddende teknik kendt som magnetisk resonansbilleddannelse virker ved at justere brintatomer i et stærkt magnetfelt og pulserende radiofrekven
Kemikere designer kemisk sonde til at registrere små temperaturændringer i kroppenKredit:Colorado State University Den ikke-invasive, livreddende teknik kendt som magnetisk resonansbilleddannelse virker ved at justere brintatomer i et stærkt magnetfelt og pulserende radiofrekven -
 Nye ringslutningsreaktioner til syntetisering af makrocykliske lægemiddelledningerIntegreret robotarbejdsstation brugt på EPFLs Biomolecular Screening Facility til at udføre kombinatorisk syntese af makrocykler og efterfølgende high-throughput målbaserede screeningsassays. Kredit:A
Nye ringslutningsreaktioner til syntetisering af makrocykliske lægemiddelledningerIntegreret robotarbejdsstation brugt på EPFLs Biomolecular Screening Facility til at udføre kombinatorisk syntese af makrocykler og efterfølgende high-throughput målbaserede screeningsassays. Kredit:A
- Hvad vejer mere vand eller luft?
- Hvordan videnskab er relateret til historie?
- Hvad er molfraktionen af oxygengas i luft?
- Er der lige så mange absorptionslinjer i solspektret er elementer, der er til stede sol?
- Ny metode kunne afsløre, hvilke gener der blev arvet fra neandertalere
- Spiropyran-funktionaliserede fotokromiske nylonbånd til langtidsføling af ultraviolet lys


