Hvad sker der med kobber II -nitrat, når det opvarmes?
trin 1:lavere temperatur (ca. 170 ° C)
* reaktion: Cu (no₃) ₂ (S) → Cuo (s) + 2no₂ (g) + ½o₂ (g)
* Forklaring: Kobber (II) nitrat nedbrydes til kobber (II) oxid (CuO), nitrogendioxidgas (NO₂) og iltgas (O₂). Denne reaktion er eksoterm, hvilket betyder, at den frigiver varme.
Trin 2:Højere temperatur (over 300 ° C)
* reaktion: Cuo (S) + NO₂ (G) → Cu (S) + ½O₂ (G) + NO₂ (G)
* Forklaring: Ved højere temperaturer nedbrydes kobber (II) oxid yderligere til kobbermetal (Cu), iltgas og nitrogendioxid. Denne reaktion er også eksotermisk.
Generelt er de endelige produkter af opvarmning af kobber (II) nitrat:
* kobbermetal (CU) :Dette er et rødbrunt fast stof.
* nitrogendioxid (ingen₂) :Dette er en rødbrun gas med en skarp lugt.
* iltgas (O₂) :Dette er en farveløs og lugtfri gas.
Observationer:
* farveændring: Oprindeligt er kobber (II) nitratet blåt. Når det nedbrydes, farve de faste ændringer til sort (Cuo) og derefter til sidst til rødbrun (Cu).
* Gasudvikling: Frigivelsen af nitrogendioxid og iltgas er tydelig, da brune dampe ses, der kommer ud af den opvarmede prøve.
sikkerhed:
* Nedbrydningen af kobber (II) nitrat producerer giftige gasser. Det er vigtigt at udføre dette eksperiment i et godt ventileret område.
* Kvælstofdioxid er en luftvejsirriterende. Det er vigtigt at undgå at indånde dampene.
I resumé resulterer opvarmning af kobber (II) nitrat i dens nedbrydning til kobbermetal, nitrogendioxid og iltgas, ledsaget af en farveændring og frigivelse af brune dampe.
Sidste artikelHvad er formlen for sølvcarbonat?
Næste artikelHvad er to vigtigste måder, hvorpå mineralform er?
 Varme artikler
Varme artikler
-
 Forskere laver protonpumpe af respiratoriske kæder i kunstig polymermembranElektronmikroskopiske billeder af en naturlig cellemembran (øverst) og polymeren PDMS-g-PEO (nederst) (højre:forstørrelse):Cellemembraner består af et lipidlag, hvori proteiner er indlejret. I modsætn
Forskere laver protonpumpe af respiratoriske kæder i kunstig polymermembranElektronmikroskopiske billeder af en naturlig cellemembran (øverst) og polymeren PDMS-g-PEO (nederst) (højre:forstørrelse):Cellemembraner består af et lipidlag, hvori proteiner er indlejret. I modsætn -
 Flygtige overraskelser opstår ved fjernelse af overskydende brintSimulerede krystalstrukturer af jomfru-DEB og T4H-DEB (kemisk kendt som 1, 4-distyrylbenzen, en trans-isomer af DEB-mellemprodukt efter indfangning af første 4 atombrint med 2 CH-bindinger på modsatte
Flygtige overraskelser opstår ved fjernelse af overskydende brintSimulerede krystalstrukturer af jomfru-DEB og T4H-DEB (kemisk kendt som 1, 4-distyrylbenzen, en trans-isomer af DEB-mellemprodukt efter indfangning af første 4 atombrint med 2 CH-bindinger på modsatte -
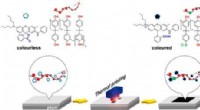 Et skridt i retning af at kvitte register kvitteringer af BPAKredit:American Chemical Society Selvom USA og andre lande har forbudt eller begrænset brugen af bisphenol A (BPA) på grund af miljø- og sundhedsmæssige bekymringer, det bruges stadig i termotry
Et skridt i retning af at kvitte register kvitteringer af BPAKredit:American Chemical Society Selvom USA og andre lande har forbudt eller begrænset brugen af bisphenol A (BPA) på grund af miljø- og sundhedsmæssige bekymringer, det bruges stadig i termotry -
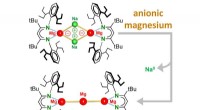 Forskere rapporterer omvendt magnesiumkemi opdagelseBillede:Harder Group Kemikere ved Friedrich-Alexander-Universitetet Erlangen-Nürnberg har offentliggjort et gennembrud inden for magnesiumkemi i tidsskriftet Natur . Magnesium (Mg) er et jordri
Forskere rapporterer omvendt magnesiumkemi opdagelseBillede:Harder Group Kemikere ved Friedrich-Alexander-Universitetet Erlangen-Nürnberg har offentliggjort et gennembrud inden for magnesiumkemi i tidsskriftet Natur . Magnesium (Mg) er et jordri
- Hvor mange forskellige energier er der?
- Et hurtigere enkeltpixelkamera:Ny teknik reducerer i høj grad antallet af eksponeringer, der er nø…
- Ændrer tiden hastigheden?
- Hvad er den hotteste del af solsystemet?
- Glødende gasskyer, der til sidst bliver stjerner?
- Slangebid? Kemikere finder ud af, hvordan man nemt og billigt kan standse giftspredning


