Hvad er formlen, når du limning af kulstof og klor?
* et kloratom: ch₃cl (methylchlorid) - Her danner kulstof fire enkeltbindinger, en med hvert hydrogenatom og et med kloratomet.
* to kloratomer: ch₂cl₂ (dichlormethan) - Kulstof danner to enkeltbindinger med brintatomer og to enkeltbindinger med kloratomer.
* tre kloratomer: chcl₃ (Chloroform) - Kulstof danner en enkelt binding med et hydrogenatom og tre enkeltbindinger med kloratomer.
* fire kloratomer: ccl₄ (Carbon Tetrachlorid) - Kulstof danner fire enkeltbindinger med kloratomer.
Generelt:
* Carbon danner altid fire obligationer.
* Klor danner altid en binding.
Disse formler er baseret på begrebet valenselektroner , som er elektronerne i den yderste skal af et atom. Carbon har fire valenselektroner, mens klor har syv. Ved at dele elektroner kan begge atomer opnå en stabil oktet (otte elektroner) i deres yderste skaller.
 Varme artikler
Varme artikler
-
 Forskere patenterer hurtige tests for kokainFIU biokemi Ph.D. studerende Haixiang Yu, kemi Ph.D. studerende Juan Canoura, og nyuddannet Obtin Alkhamis offentliggjorde en undersøgelse af FIUs patenterede kokaindetektionsteknologier. Kredit:Flori
Forskere patenterer hurtige tests for kokainFIU biokemi Ph.D. studerende Haixiang Yu, kemi Ph.D. studerende Juan Canoura, og nyuddannet Obtin Alkhamis offentliggjorde en undersøgelse af FIUs patenterede kokaindetektionsteknologier. Kredit:Flori -
 Forskning i brugsklar terapeutisk mad søger drastisk reduktion af dødsfald som følge af alvorlig …MIT kandidatstuderende Tonghan Gu (til højre) arbejder med teknikere på en facilitet i Vasai, Indien, at producere et parti brugsklare terapeutiske fødevarer i pulverform. Formlen, han har udviklet, b
Forskning i brugsklar terapeutisk mad søger drastisk reduktion af dødsfald som følge af alvorlig …MIT kandidatstuderende Tonghan Gu (til højre) arbejder med teknikere på en facilitet i Vasai, Indien, at producere et parti brugsklare terapeutiske fødevarer i pulverform. Formlen, han har udviklet, b -
 Kemikere opdager, hvordan blåt lys fremskynder blindhedDr. Ajith Karunarathne undersøgte giftig iltgenerering af retinal under eksponering for blåt lys. Kredit:Dan Miller, Universitetet i Toledo Blåt lys fra digitale enheder og solen forvandler vitale
Kemikere opdager, hvordan blåt lys fremskynder blindhedDr. Ajith Karunarathne undersøgte giftig iltgenerering af retinal under eksponering for blåt lys. Kredit:Dan Miller, Universitetet i Toledo Blåt lys fra digitale enheder og solen forvandler vitale -
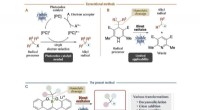 Ny protokol for organisk syntese ved hjælp af organoboronforbindelser og synligt lysSammenligning af konventionelle metoder og den foreliggende metode Credit:Kanazawa University Alkylradikaler er carbonradikaler af normale og forgrenede alkaner, tilgængelig som reaktionsmellempro
Ny protokol for organisk syntese ved hjælp af organoboronforbindelser og synligt lysSammenligning af konventionelle metoder og den foreliggende metode Credit:Kanazawa University Alkylradikaler er carbonradikaler af normale og forgrenede alkaner, tilgængelig som reaktionsmellempro
- Hvis der anvendes lige kræfter på en let og tung genstand, hvilken vil man fremskynde mere?
- Forskere udvikler helt optiske switches, der kan føre til hurtigere computerprocessorer
- Effekt af pH på et molekyle?
- Hvad er et virkeligt eksempel på acceleration?
- Plastikædende bakterier gør affald til nyttige udgangsmaterialer til andre produkter
- Hvad er eksempler på indirekte energiforbrug?


