Hvilket metalhydroxid er mest opløseligt i vand?
Her er hvorfor:
* opløselighedstendenser: Opløselighed af metalhydroxider øger generelt en gruppe i den periodiske tabel. Dette skyldes, at størrelsen på metalkationen øges, hvilket fører til svagere tiltrækning mellem kationen og hydroxidanionen.
* Bariums position: Barium er placeret i gruppe 2 (alkaliske jordmetaller) og er den største af de almindelige alkaliske jordmetaller.
* Andre faktorer: Mens størrelse er en vigtig faktor, spiller andre faktorer som ladning af metalkationen og stabiliteten af hydroxidanionen også en rolle.
Vigtig note: Selvom bariumhydroxid er det mest opløselige metalhydroxid, betragtes det stadig som en stærk base og bør håndteres med forsigtighed.
 Varme artikler
Varme artikler
-
 Datakraft løser molekylært mysteriumForskere måtte studere næsten 100, 000 simuleringsbilleder af denne type, før de kunne identificere, hvad der får vandmolekylerne til at splitte. Masser af computerkraft gik til disse simuleringer. Kr
Datakraft løser molekylært mysteriumForskere måtte studere næsten 100, 000 simuleringsbilleder af denne type, før de kunne identificere, hvad der får vandmolekylerne til at splitte. Masser af computerkraft gik til disse simuleringer. Kr -
 En blidere, mere præcis laserskæringsteknikPac-Man udskæring ved laserskæring. Kredit:H. Borchers et al. Laserskæringsteknikker drives normalt af højenergistråler, så varme, at de smelter de fleste materialer. Nu har forskere fra McGill Uni
En blidere, mere præcis laserskæringsteknikPac-Man udskæring ved laserskæring. Kredit:H. Borchers et al. Laserskæringsteknikker drives normalt af højenergistråler, så varme, at de smelter de fleste materialer. Nu har forskere fra McGill Uni -
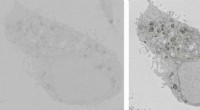 Smart trick muliggør 20 gange hurtigere billeddannelse med elektronmikroskopiTo billeder af en HeLa-celle, begge optaget på 33,6 sekunder. Billedet til højre blev taget, mens en spænding blev påført prøveholderen. Kredit:TU Delft Forskere ved Delft University of Technology
Smart trick muliggør 20 gange hurtigere billeddannelse med elektronmikroskopiTo billeder af en HeLa-celle, begge optaget på 33,6 sekunder. Billedet til højre blev taget, mens en spænding blev påført prøveholderen. Kredit:TU Delft Forskere ved Delft University of Technology -
 Protein afledt af havre bindes til celle-selvmordsenzym i ny teknikKredit:CC0 Public Domain Evnen til selektivt at udrydde bestemte celletyper fra flercellede organismer gør det muligt for forskere at dechiffrere disse cellers funktioner, men de tilgængelige værk
Protein afledt af havre bindes til celle-selvmordsenzym i ny teknikKredit:CC0 Public Domain Evnen til selektivt at udrydde bestemte celletyper fra flercellede organismer gør det muligt for forskere at dechiffrere disse cellers funktioner, men de tilgængelige værk
- Hvad blev de tidligste fossiler fundet i hestefamilien?
- Hvor mange øre svarer til en million dollars skriver svaret i videnskabelig notation?
- Hvad er impulsen af et objekt, der anvender 30 N i 4 sekunder?
- Ny model viser, hvordan vores sociale netværk kan bidrage til at skabe økonomiske fænomener
- Hvilket er lettere regenter fysik eller kemi?
- Hvad er produktet, når magnesium reagerer med nitrogen?


