Formerer jod og nitrogen en ionisk forbindelse?
* Elektronegativitet: Jod og nitrogen har relativt ens elektronegativitetsværdier. Nitrogen er mere elektronegativ end jod (3,04 vs. 2,66), men forskellen er ikke stor nok til at skabe en fuld overførsel af elektroner, der er nødvendige for en ionisk binding.
* limningstype: Bindingen mellem jod og nitrogen er mere tilbøjelig til at være kovalent, hvor elektroner deles snarere end overført. Dette skyldes, at elektronegativitetsforskellen er tættere på området, der typisk er forbundet med kovalente bindinger.
* stabilitet: Mens der er nogle forbindelser med nitrogen-iod-bindinger, er de typisk mindre stabile og nedbrydes ofte let. Dette skyldes den lignende elektronegativitet og den relativt svage binding mellem disse elementer.
Derfor, mens jod og nitrogen kan danne forbindelser, er det usandsynligt, at de danner en typisk ionisk forbindelse.
Sidste artikelEr lithium og fluorionisk eller kovalent?
Næste artikelEr der sandsynligvis en ionisk forbindelse mellem fluor og klor?
 Varme artikler
Varme artikler
-
 Forskere skaber syntetisk prototissue, der kan synkroniseresOpdagelsen, udgivet i Naturmaterialer , er den første kemisk programmerede tilgang til fremstilling af et kunstigt væv. Fundene, som kan have store sundhedsmæssige anvendelser i fremtiden, kunne se
Forskere skaber syntetisk prototissue, der kan synkroniseresOpdagelsen, udgivet i Naturmaterialer , er den første kemisk programmerede tilgang til fremstilling af et kunstigt væv. Fundene, som kan have store sundhedsmæssige anvendelser i fremtiden, kunne se -
 Udfiskning af de dårlige æbler:Ny kvantitativ metode til at vurdere fødevaresikkerhedenForkælet mad, især fisk, kan have høje niveauer af histamin, som kan være farligt for mennesker; dermed, det er vigtigt at udtænke metoder til påvisning af sådanne skadelige kemikalier i fødevarer Kre
Udfiskning af de dårlige æbler:Ny kvantitativ metode til at vurdere fødevaresikkerhedenForkælet mad, især fisk, kan have høje niveauer af histamin, som kan være farligt for mennesker; dermed, det er vigtigt at udtænke metoder til påvisning af sådanne skadelige kemikalier i fødevarer Kre -
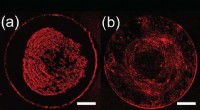 Ny fremstillingsteknik kan forbedre det almindelige problem inden for printteknologiFor figur A, der er partikeltransport til spidsen af måldråben, og der dannes en tæt midteraflejring. For figur B, den endelige kortlagte indbetaling er mere ensartet. Kredit: Langmuir En ny fr
Ny fremstillingsteknik kan forbedre det almindelige problem inden for printteknologiFor figur A, der er partikeltransport til spidsen af måldråben, og der dannes en tæt midteraflejring. For figur B, den endelige kortlagte indbetaling er mere ensartet. Kredit: Langmuir En ny fr -
 Nye automatiserede biologiske prøveanalysesystemer til at fremskynde sygdomsopdagelseIllustration af de anvendte matematiske transformationer, først på billedet af et skakbræt, derefter på mikrofluidiske multipoler. Kredit:Polytechnique Montréal og McGill University Professor Thom
Nye automatiserede biologiske prøveanalysesystemer til at fremskynde sygdomsopdagelseIllustration af de anvendte matematiske transformationer, først på billedet af et skakbræt, derefter på mikrofluidiske multipoler. Kredit:Polytechnique Montréal og McGill University Professor Thom
- Hvordan den altruistiske reaktion på optøjer til yderste højre afslører medfødt godhed hos menn…
- Hvad er den type uoverensstemmelse, hvorpå der findes en erosionsoverflade, et adskillige vandrette…
- Hvilken geologisk proces finder sted ved en oceanisk kontinentalpladegrænse?
- Pink Quartz Betydning:Et kig på den ægte kærlighedssten
- Hvad er komplette jord 3 lag?
- Hvorfor March Madness er en særlig tid på året for statsbudgetterne


