Sammenlign de relative polariteter af OH-binding og NH-binding?
* Elektronegativitet: Oxygen er mere elektronegativ end nitrogen. Dette betyder, at ilt har et stærkere træk på delte elektroner i en binding.
* Forskel i elektronegativitet: Forskellen i elektronegativitet mellem ilt og brint (3,44 - 2,20 =1,24) er større end forskellen mellem nitrogen og brint (3,04 - 2,20 =0,84).
* dipolmoment: Den større elektronegativitetsforskel i OH -bindingen resulterer i en større delvis negativ ladning på iltatomet og en større delvis positiv ladning på hydrogenatomet. Dette skaber et større dipolmoment, hvilket indikerer en stærkere polaritet.
Kortfattet:
* OH -bindingen er mere polær på grund af den større elektronegativitet af ilt sammenlignet med nitrogen, hvilket fører til et større dipolmoment.
* Dette betyder, at elektronerne i OH -bindingen er stærkere trukket mod iltatomet, hvilket skaber en større adskillelse af ladning.
 Varme artikler
Varme artikler
-
 En vej til at undgå defekter under additiv fremstillingKunstværk, der viser grænsen og oprindelsen for nøglehulsporøsitet. På venstre side af figuren, nøglehullets porøsitetsgrænse i laserkraften – scanningshastighedsrummet er skarpt og glat. På den højre
En vej til at undgå defekter under additiv fremstillingKunstværk, der viser grænsen og oprindelsen for nøglehulsporøsitet. På venstre side af figuren, nøglehullets porøsitetsgrænse i laserkraften – scanningshastighedsrummet er skarpt og glat. På den højre -
 Bygninger – Beton på det dobbelteORNL forskere brugte fiberforstærkninger lavet af stål, glas og kulstof for at udvikle en betonblanding, der viste høj tidlig styrke inden for seks timer efter produktion, som er nødvendig for den præ
Bygninger – Beton på det dobbelteORNL forskere brugte fiberforstærkninger lavet af stål, glas og kulstof for at udvikle en betonblanding, der viste høj tidlig styrke inden for seks timer efter produktion, som er nødvendig for den præ -
 Fra medicin til nanoteknologi:Hvordan guld stille og roligt former vores verdenKredit:itti ratanakiranaworn/Shutterstock Det periodiske system med kemiske grundstoffer fylder 150 i år. Jubilæet er en chance for at skinne lys over bestemte elementer - hvoraf nogle virker alle
Fra medicin til nanoteknologi:Hvordan guld stille og roligt former vores verdenKredit:itti ratanakiranaworn/Shutterstock Det periodiske system med kemiske grundstoffer fylder 150 i år. Jubilæet er en chance for at skinne lys over bestemte elementer - hvoraf nogle virker alle -
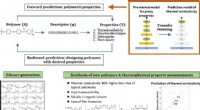 Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM],
Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM],
- Hvordan produceres helium i stjerner?
- Hvilket geografitema er folk først bosat der for over 8000 år siden?
- Hvordan bruger du et refraktorteleskop effektivt til stargazing og observation af himmelobjekter?
- Elektrokemisk syntese nu mulig uden elektrisk strømkilde
- Hvad vejer mere 1 DM3 af ammoniak eller hydrogenchloridgas?
- At finde årsagen til kapacitetstab i et metaloxid-batterimateriale


