Hvorfor smelter is ved en lavere temperatur med salt?
Videnskaben om frysepunktdepression
* salt opløses i vand: Når salt (natriumchlorid, NaCl) tilsættes til vand, opløses det i dets ioner (Na+ og Cl-).
* Forstyrrelse af vandstruktur: Disse ioner forstyrrer dannelsen af de normale hydrogenbindinger mellem vandmolekyler. Dette forstyrrer den regelmæssige, krystallinske isstruktur.
* sænkning af frysepunkt: For at fryse er vandmolekyler nødt til at danne disse organiserede brintbindinger. Tilstedeværelsen af saltioner gør det sværere for dem at danne disse bindinger, hvilket kræver en lavere temperatur for vandet at fryse.
hvordan det fungerer detaljeret:
1. salt opløses: Salt opløses i det tynde lag af flydende vand, der altid findes på isoverfladen.
2. ioner forstyrrer obligationer: De opløste ioner kommer i vejen for vandmolekylerne, der prøver at danne den organiserede isstruktur.
3. vand skal afkøles yderligere: For at fryse skal vandmolekylerne afkøles yderligere for at kompensere for forstyrrelsen forårsaget af saltioner. Dette resulterer i et lavere frysepunkt.
Vigtig note: Mængden af tilsat salt påvirker depressionen på frysepunktet. Mere salt betyder et lavere frysepunkt. Der er dog en grænse for, hvor meget salt du kan opløse i vand.
Virkelige applikationer:
* de-icing veje: Salt bruges ofte til at smelte is på veje og fortove.
* laver is: Salt tilsættes til isbadet hos isproducenter for at sænke isens frysepunkt, hvilket hjælper med at fryse isen hurtigere.
Fortæl mig, hvis du gerne vil have en mere detaljeret forklaring af et specifikt aspekt!
 Varme artikler
Varme artikler
-
 Enkel og billig revneheling af keramikbaserede kompositterFig. 1:Udbredelse af indført revne i Al2O3/Ti-komposit (a) og helede revner efter anodisering ved stuetemperatur (b, c og d), hvor revner ved dispergeret titanium (hvide partikler) samt en del af revn
Enkel og billig revneheling af keramikbaserede kompositterFig. 1:Udbredelse af indført revne i Al2O3/Ti-komposit (a) og helede revner efter anodisering ved stuetemperatur (b, c og d), hvor revner ved dispergeret titanium (hvide partikler) samt en del af revn -
 Ny teknik, hvor lægemidler får bakterier til at lyse, kan hjælpe med at bekæmpe antibiotikaresis…Lægemiddeloptagelse i bakterier før og efter. Kredit:Dr Stefano Pagliara, University of Exeter En ny teknik kan hjælpe med at reducere antibiotikaudskrivning ved at forudsige, hvilke lægemidler de
Ny teknik, hvor lægemidler får bakterier til at lyse, kan hjælpe med at bekæmpe antibiotikaresis…Lægemiddeloptagelse i bakterier før og efter. Kredit:Dr Stefano Pagliara, University of Exeter En ny teknik kan hjælpe med at reducere antibiotikaudskrivning ved at forudsige, hvilke lægemidler de -
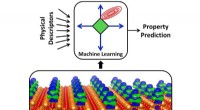 Undersøgelse viser, at maskinlæring kan forbedre katalytisk designEn kvantekemisk simulering (nederste panel) viser ladningsoverførslen (blå/grøn) mellem metalatomer og en underliggende støtte (orange). Dette er kun én beskrivelse af en katalysators fysiske adfærd,
Undersøgelse viser, at maskinlæring kan forbedre katalytisk designEn kvantekemisk simulering (nederste panel) viser ladningsoverførslen (blå/grøn) mellem metalatomer og en underliggende støtte (orange). Dette er kun én beskrivelse af en katalysators fysiske adfærd, -
 Nyt materiale slår verdensrekord for at omdanne varme til elektricitetProf. Ernst Bauer i laboratoriet. Kredit:TU Wien En ny type materiale genererer elektrisk strøm meget effektivt fra temperaturforskelle. Dette giver sensorer og små processorer mulighed for at for
Nyt materiale slår verdensrekord for at omdanne varme til elektricitetProf. Ernst Bauer i laboratoriet. Kredit:TU Wien En ny type materiale genererer elektrisk strøm meget effektivt fra temperaturforskelle. Dette giver sensorer og små processorer mulighed for at for
- Hvad er accelerationen af et faldende objekt, der har nået terminalhastighed?
- Hvordan ændrer WeatheringRosion og deponering jord?
- Sådan konverteres milligram pr. Liter til Molarity
- Trump trækker forureningsreglerne tilbage for boring på amerikanske jorder
- Hvordan holder himlen solen op i luften?
- Waymo kortlægger L.A. i håb om en dag at introducere førerløse taxaer


