Den kemiske reaktion mellem kobberoxid og kulstof, der producerer dioxid, er et eksempel på?
* reduktion: Kobberoxid (CUO) reduceres. Kobberet i oxid får elektroner, og dets oxidationstilstand falder fra +2 til 0. Dette er repræsenteret af følgende halvreaktion:
* Cuo + 2e- → Cu + O2-
* Oxidation: Carbon (C) oxideres. Det mister elektroner, og dens oxidationstilstand stiger fra 0 til +4. Dette er repræsenteret af følgende halvreaktion:
* C → CO2 + 4E-
samlet reaktion:
Cuo + C → Cu + CO2
I denne reaktion fungerer kobberoxid som et oxidationsmiddel (det accepterer elektroner), og kulstof fungerer som et reducerende middel (det donerer elektroner).
Sidste artikelHvad er den molære masse af Mercurous Nitrate Hg2NO3 2?
Næste artikelHvad er en kemisk reaktant som reaktion?
 Varme artikler
Varme artikler
-
 Brug af virtual reality-systemer til at undervise i kemi i 3-DEn abstrakt repræsentation af de fodboldformede buckminsterfulleren-molekyler i virtual reality. Kredit:Mike OConnor, i samarbejde med Interactive Scientific Ltd, under CC BY-ND 4.0. Et team af fo
Brug af virtual reality-systemer til at undervise i kemi i 3-DEn abstrakt repræsentation af de fodboldformede buckminsterfulleren-molekyler i virtual reality. Kredit:Mike OConnor, i samarbejde med Interactive Scientific Ltd, under CC BY-ND 4.0. Et team af fo -
 Adsorberende materiale filtrerer giftigt krom, arsen fra vandforsyningerForskere ved Oak Ridge National Laboratory designet et adsorberende materiale til hurtigt at fjerne giftigt krom og arsen på samme tid fra vandressourcer. Kredit:Adam Malin/ORNL, U.S. Dept. of Energy
Adsorberende materiale filtrerer giftigt krom, arsen fra vandforsyningerForskere ved Oak Ridge National Laboratory designet et adsorberende materiale til hurtigt at fjerne giftigt krom og arsen på samme tid fra vandressourcer. Kredit:Adam Malin/ORNL, U.S. Dept. of Energy -
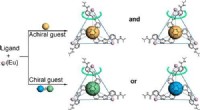 Forskere opnår gæstedrevet selvsamling og chiral induktion af fotofunktionelle lanthanid-tetraedri…Kredit:Chinese Academy of Sciences Chirale koordinationsbure har potentielle anvendelser inden for enantioselektiv genkendelse, sansning og symmetrisk katalyse. Generelt kan chirale koordinationsbu
Forskere opnår gæstedrevet selvsamling og chiral induktion af fotofunktionelle lanthanid-tetraedri…Kredit:Chinese Academy of Sciences Chirale koordinationsbure har potentielle anvendelser inden for enantioselektiv genkendelse, sansning og symmetrisk katalyse. Generelt kan chirale koordinationsbu -
 Kaffeforfalskning afdækket ved hjælp af ny metodeKredit:Quadram Institute Forskere fra Quadram Institute har udviklet en ny teknik til at skelne mellem overlegen Arabica -kaffe og billigere, lavere kvalitet Robusta. Ved hjælp af den nye teknik,
Kaffeforfalskning afdækket ved hjælp af ny metodeKredit:Quadram Institute Forskere fra Quadram Institute har udviklet en ny teknik til at skelne mellem overlegen Arabica -kaffe og billigere, lavere kvalitet Robusta. Ved hjælp af den nye teknik,
- Billede:Hubble fanger en funklende klynge
- Redde bierne? Der er en app til det
- Hvor mange officielle konstellationer har identificeret?
- Hvilke enheder bruges til at måle vægt og masse Hvordan fungerer de?
- Genetikere opdager to forskellige måder for transkriptionsterminering
- Hvorfor er solens ultimative energikilde for alle levende ting?


