Er sukker mere opløseligt end kobbersulfat?
* Polaritet: Sukker er et meget polært molekyle på grund af tilstedeværelsen af mange hydroxylgrupper (-OH). Vand er også et polært molekyle. "Som opløser som", hvilket betyder, at polære stoffer opløses godt i andre polære stoffer.
* Intermolekylære kræfter: Sukker danner stærke brintbindinger med vandmolekyler, hvilket hjælper det med at opløses let. Kobbersulfat, selvom det er noget polært, danner svagere interaktioner med vand.
* opløselighedsdata:
* sukker (saccharose): Cirka 200 gram sukker kan opløses i 100 gram vand ved stuetemperatur.
* kobbersulfat: Kun ca. 20 gram kobbersulfat kan opløses i 100 gram vand ved stuetemperatur.
Derfor gør sukkerets høje polaritet, stærke interaktioner med vand og højere opløselighedsværdier det meget mere opløseligt end kobbersulfat.
 Varme artikler
Varme artikler
-
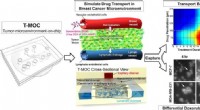 Mikrofluidisk anordning simulerer kræftbehandling lige så effektivt som forskningsdyrDenne grafik viser, hvordan en ny teknologi udviklet på Purdue University, der simulerer tumorer. Kredit:Purdue University foto/Altug Ozcelikkale En ny teknologi, der simulerer tumorer, har vist s
Mikrofluidisk anordning simulerer kræftbehandling lige så effektivt som forskningsdyrDenne grafik viser, hvordan en ny teknologi udviklet på Purdue University, der simulerer tumorer. Kredit:Purdue University foto/Altug Ozcelikkale En ny teknologi, der simulerer tumorer, har vist s -
 Forskere løser kontroverser om energigabet i Van der Waals-materialeTeYu Chien, en University of Wyoming lektor i fysik og astronomi, og Dinesh Baral, en UW kandidatstuderende, ledet forskning, der brugte scanning tunneling mikroskopi og spektroskopi målinger, der kla
Forskere løser kontroverser om energigabet i Van der Waals-materialeTeYu Chien, en University of Wyoming lektor i fysik og astronomi, og Dinesh Baral, en UW kandidatstuderende, ledet forskning, der brugte scanning tunneling mikroskopi og spektroskopi målinger, der kla -
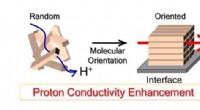 Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri
Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri -
 Brug af neutroner og røntgenstråler til at analysere ældningen af lithiumbatterierRøntgentomografien viser brud (sort) i områderne af elektriske kontakter (hvide). Kredit:T.Arlt, I. Manke/HZB, R. Ziesche/UCL Lithium-batterier driver smartphones, bærbare computere, og elektriske
Brug af neutroner og røntgenstråler til at analysere ældningen af lithiumbatterierRøntgentomografien viser brud (sort) i områderne af elektriske kontakter (hvide). Kredit:T.Arlt, I. Manke/HZB, R. Ziesche/UCL Lithium-batterier driver smartphones, bærbare computere, og elektriske
- Månens guldfeber kan skabe konflikt på jorden, hvis vi ikke handler nu - ny forskning
- Mikrobølgebaseret testmetode kan hjælpe med at holde 3-D-chipdesigners øjne åbne
- Ulve på et fly:Hvordan helligdommen fik 4 kritisk truede hvalpe i gang igen
- Hvad er forskellen mellem fysisk afstand og tidsafstand?
- Hvordan kombineres atomer for at fremstille forbindelser?
- Hvilken del af solsystemet kan tage op til 30 millioner års bane -sol?


