Mikrofluidisk anordning simulerer kræftbehandling lige så effektivt som forskningsdyr
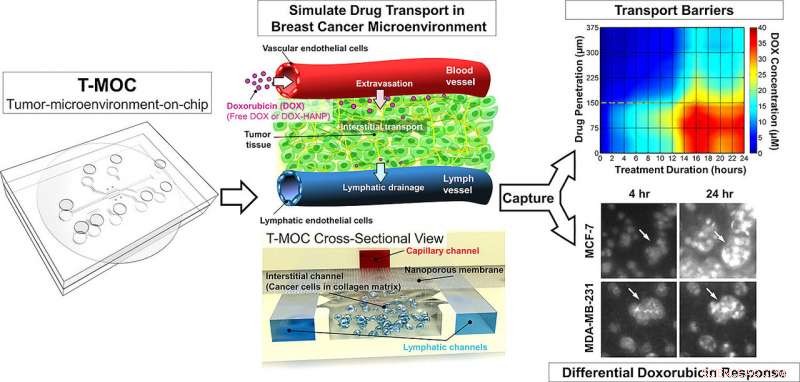
Denne grafik viser, hvordan en ny teknologi udviklet på Purdue University, der simulerer tumorer. Kredit:Purdue University foto/Altug Ozcelikkale
En ny teknologi, der simulerer tumorer, har vist sig at fungere lige så godt som at forske dyr i at teste kemoterapimedicin, repræsenterer et potentielt værktøj til screening af lægemidler før behandling af en patient.
Et langsigtet mål er at inkorporere biopsierede cancerceller fra patienter og teste effektiviteten af forskellige lægemidler på de patient-afledte celler, sagde Bumsoo Han, en Purdue University professor i mekanisk og biomedicinsk teknik.
"Der er mange forskellige typer kemoterapimedicin, så klinikere kan være i stand til at indsnævre, hvilke der sandsynligvis vil være mere effektive end andre, " sagde han. "Succesfuld lægemiddellevering og overvindelse af lægemiddelresistens er de primære kliniske udfordringer for håndtering og behandling af kræft. For at løse dette problem, vi udviklede tumor-mikromiljø-på-chip (T-MOC)."
Enheden er omkring 4,5 centimeter (1,8 tommer) kvadratisk og indeholder "mikrofluidiske" kanaler, hvor cancerceller dyrkes i en tredimensionel "ekstracellulær matrix, " et stilladslignende materiale fundet mellem celler i levende væv. Eksperimenterne inkorporerer også "interstitiel væske, " som findes inde i tumorer og menes at være en barriere for lægemiddellevering.
Et sådant værktøj kunne bruges til "præcisionsmedicin, " hvor lægemiddelbehandling er skræddersyet til individuelle patienter og visse kræfttyper. Lægemiddelresistens og forskellige undertyper af tumorer repræsenterer kritiske flaskehalse for effektiv kemoterapi. Kræftceller producerer multiresistente proteiner, der pumper anti-cancer-lægemidlerne ud af cellerne, hjælpe dem med at overleve kemoterapibehandling.
Forskningen har til formål at udvikle en lægemiddelscreeningsplatform til at efterligne disse multiple lægemiddelresistensmekanismer, samt at validere resultaterne i forhold til den nuværende guldstandard, forskning med små dyr, sagde Han.
Nye forskningsresultater blev beskrevet i et papir, der skal offentliggøres i november i Journal of Controlled Release . Artiklens hovedforfatter er Purdue postdoktorale forskningsassocierede Altug Ozcelikkale.
Forskerne brugte det almindelige kemoterapi-lægemiddel doxorubicin og testede også forskellen mellem doxorubicin i konventionel form versus en formulering af nanopartikler.
Artiklen var medforfatter af forskere tilknyttet Purdue's School of Mechanical Engineering, Institut for Komparativ Patobiologi, Center for Kræftforskning, Weldon School of Biomedical Engineering og Birck Nanotechnology Center; Indiana Universitys afdeling for farmakologi og toksikologi; og det biomedicinske forskningsinstitut ved Korea Institute of Science and Technology. En liste over medforfattere er inkluderet i abstraktet.
Forskerne har tidligere vist, at T-MOC-enheden var i stand til at skelne mellem forskellige typer kræftceller. I de nye resultater, holdet viste, at T-MOC udførte såvel som forskning mus i at teste effektiviteten af anti-cancer lægemidler på to typer brystkræftceller, kaldet MCF-7 og MDA-MB-231. I øvrigt, den molekylære mekanisme for doxorubicinresistens var i overensstemmelse med musens, sagde Han.
Resultaterne viste også, at T-MOC er i stand til at simulere "plasma clearance, "en kropsreaktion, hvor kræftmedicin filtreres af leveren og nyrerne, tillader kun en lille mængde at nå tumoren.
Begge cellelinjer dyrket på T-MOC viste øget resistens over for lægemidlerne sammenlignet med celler dyrket på en standard flad petriskålkultur, matcher resultaterne med mus og foreslår et mere naturtro resultat.
"Dette bekræfter T-MOC's forudsigelige evne til in vivo lægemiddelrespons, Han sagde. "Denne indledende karakterisering af T-MOC indikerer dets transformative potentiale til at teste lægemiddeleffektivitet."
Fremtidigt arbejde vil udvide forskningen i forskellige kræfttyper, herunder bugspytkirtel- og prostatacancer.
Sidste artikelDioxan-chomping mikrobe har et nyttigt gen
Næste artikelSMART:Ansigtsgenkendelse for molekylære strukturer
 Varme artikler
Varme artikler
-
 Neutroner fanger formskiftende coronavirus-proteinkompleks på aktenKredit:Oak Ridge National Laboratory Mens alle vira har nogle midler til at bekæmpe kroppens immunsystem, forskere har undersøgt, hvordan SARS-CoV-2-coronavirus - årsagen til den globale COVID-19-
Neutroner fanger formskiftende coronavirus-proteinkompleks på aktenKredit:Oak Ridge National Laboratory Mens alle vira har nogle midler til at bekæmpe kroppens immunsystem, forskere har undersøgt, hvordan SARS-CoV-2-coronavirus - årsagen til den globale COVID-19- -
 Omdannelse af svovldioxid fra skadelig til nyttigKredit:CC0 Public Domain Forskere har skabt molekylære bure i en polymer for at fange skadelig svovldioxidforurening for at omdanne den til nyttige forbindelser og reducere affald og emissioner.
Omdannelse af svovldioxid fra skadelig til nyttigKredit:CC0 Public Domain Forskere har skabt molekylære bure i en polymer for at fange skadelig svovldioxidforurening for at omdanne den til nyttige forbindelser og reducere affald og emissioner. -
 Kan sollys omdanne emissioner til nyttige materialer?Kredit:Pixabay/CC0 Public Domain Shaama Sharada kalder kuldioxid - den værste lovovertræder af den globale opvarmning - en meget stabil, meget glad molekyle. Det vil hun ændre på. For nylig off
Kan sollys omdanne emissioner til nyttige materialer?Kredit:Pixabay/CC0 Public Domain Shaama Sharada kalder kuldioxid - den værste lovovertræder af den globale opvarmning - en meget stabil, meget glad molekyle. Det vil hun ændre på. For nylig off -
 Bedre løsninger til fremstilling af brint kan ligge lige ved overfladenDe unikke interaktioner mellem perovskitoxid, dets skiftende overfladelag, og jernarter, der er aktive mod OER, baner en ny vej for design af aktive og stabile materialer, bringer os et skridt tættere
Bedre løsninger til fremstilling af brint kan ligge lige ved overfladenDe unikke interaktioner mellem perovskitoxid, dets skiftende overfladelag, og jernarter, der er aktive mod OER, baner en ny vej for design af aktive og stabile materialer, bringer os et skridt tættere
- Livet i verdens tørreste ørken set som tegn på potentielt liv på Mars
- Malerier, solpletter og frostmesser:Rethinking the Little Ice Age
- Sådan beregnes isotoper
- Lab 3-D scanner menneskelige skeletrester, der går tilbage til den amerikanske borgerkrig
- Ny bog afslører, i hvilket omfang kvinder er undervurderet i globale værdikæder
- Nanorørsarmeringsjern gør grafen dobbelt så sejt


