Hvad er forskellen mellem jernatom og et natriumatom?
1. Atomnummer og struktur:
* jern (Fe): Atomnummer 26. Har 26 protoner, 26 elektroner og typisk 30 neutroner (hvilket gør sin atommasse omkring 56). Dens elektronkonfiguration er kompleks, med elektroner fordelt på flere skaller.
* natrium (NA): Atomnummer 11. Har 11 protoner, 11 elektroner og 12 neutroner (atommasse omkring 23). Dens elektronkonfiguration er enklere med en enkelt elektron i dets yderste skal.
2. Kemiske egenskaber:
* jern: Et overgangsmetal, hvilket betyder, at det kan miste elektroner på forskellige måder og danne ioner med forskellige ladninger. Kendt for sin styrke, holdbarhed og evne til at danne magnetiske materialer.
* natrium: Et alkalimetal, meget reaktivt, mister let sit enkelt ydre elektron for at danne en +1 ion (Na +). Dette gør natrium til et stærkt reduktionsmiddel.
3. Fysiske egenskaber:
* jern: Fast ved stuetemperatur, stærk, hård, god leder af varme og elektricitet, magnetisk.
* natrium: Blød, sølvhvid metal, meget reaktiv med vand og luft. Det smelter ved en lav temperatur (98 ° C).
4. Reaktivitet:
* jern: Reagerer langsomt med luft og vand og danner rust (jernoxid). Kan korroderes af syrer.
* natrium: Meget reaktiv med vand, der producerer brintgas og varme (potentielt eksplosiv). Reagerer voldsomt med syrer.
5. Anvendelser:
* jern: Brugt i byggeri, fremstilling, værktøjer, apparater og mange andre applikationer.
* natrium: Brugt til fremstilling af natriumhydroxid (Lye), natriumchlorid (bordsalt) og andre kemikalier. Brugt også i nogle lamper og atomreaktorer.
Kortfattet:
Jern og natrium er meget forskellige elementer med forskellige egenskaber på grund af deres forskellige atomstrukturer, antal elektroner og elektronkonfigurationer. Dette fører til meget forskellige reaktivitet, fysiske egenskaber og anvendelser.
 Varme artikler
Varme artikler
-
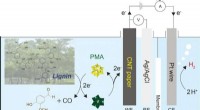 Et nyt biobrændstofsystem til brintproduktion fra biomasseSkematisk diagram af biproduktproduktion og brintudvikling gennem nedbrydning af lignin. Kredit:UNIST Der er udviklet en ny teknologi til brintproduktion fra processen, som involverer elektron, de
Et nyt biobrændstofsystem til brintproduktion fra biomasseSkematisk diagram af biproduktproduktion og brintudvikling gennem nedbrydning af lignin. Kredit:UNIST Der er udviklet en ny teknologi til brintproduktion fra processen, som involverer elektron, de -
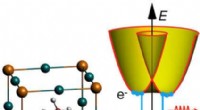 Lyser på rekombinationsmekanismer i solcellematerialerStærk spin-orbit-kobling i halogenidperovskitter inducerer spaltning af båndkanterne, hvilket kan påvirke rekombinationshastigheden. Kredit:X. Zhang og J.-X. Shen Hybride perovskiter er spektakulæ
Lyser på rekombinationsmekanismer i solcellematerialerStærk spin-orbit-kobling i halogenidperovskitter inducerer spaltning af båndkanterne, hvilket kan påvirke rekombinationshastigheden. Kredit:X. Zhang og J.-X. Shen Hybride perovskiter er spektakulæ -
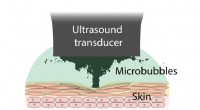 Brug af lyd og bobler til at gøre bandager mere klæbrige og holder længereUltralydsinducerede mikrobobler medierer bioadhæsion. Kredit:Zhenwei Ma Forskere har opdaget, at de kan kontrollere klæbrigheden af klæbende bandager ved hjælp af ultralydsbølger og bobler. Dette
Brug af lyd og bobler til at gøre bandager mere klæbrige og holder længereUltralydsinducerede mikrobobler medierer bioadhæsion. Kredit:Zhenwei Ma Forskere har opdaget, at de kan kontrollere klæbrigheden af klæbende bandager ved hjælp af ultralydsbølger og bobler. Dette -
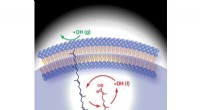 Forskere opdager et nyt spor bag aldersrelaterede sygdomme og madfordærvelseIllustration af Criegee-mellemmekanismen. Berkeley Lab-forskere har fundet en fælles sammenhæng mellem Criegee-mellemprodukter og nedbrydningen af de umættede lipider i fødevarer og cellerne i vores
Forskere opdager et nyt spor bag aldersrelaterede sygdomme og madfordærvelseIllustration af Criegee-mellemmekanismen. Berkeley Lab-forskere har fundet en fælles sammenhæng mellem Criegee-mellemprodukter og nedbrydningen af de umættede lipider i fødevarer og cellerne i vores
- Hvilken videnskabsenergi giver du en bold, når du sparker den?
- Når en bølge bøjer sig, når den går fra et medium til et andet, hvad sker der?
- Hvad bevæger luft og termisk energi gennem Troposohere?
- Nobelvindende laseropdagelser, der lyste feltet op
- Hvordan påvirker brandemissioner fra industriplantager luftkvaliteten i Ækvatorial SEA?
- Hvad er strukturformlen for tetrachlormethan?


