Hvad sker der i en reaktion, hvis det er i kemisk ligevægt?
Nøgleegenskaber ved ligevægt
* satser er ens: Den fremadrettede reaktionshastighed (reaktanter, der bliver til produkter), er lig med den omvendte reaktionshastighed (produkter, der vender tilbage til reaktanter). Dette betyder, at koncentrationerne af reaktanter og produkter forbliver konstante over tid.
* nettoændring er nul: Mens individuelle reaktioner stadig forekommer, er den samlede ændring i systemet nul. Der er ingen observerbar ændring i mængderne af reaktanter eller produkter.
* Dynamisk proces: Ligevægt er ikke en statisk tilstand. Reaktioner fortsætter med at ske, men i et lige så stort tempo i begge retninger. Det er som en trækkraft, hvor begge sider trækker med lige kraft, hvilket resulterer i ingen bevægelse.
Hvad sker der ikke ved ligevægt
* reaktioner stopper: Reaktioner forekommer fortsat, bare med lige store hastigheder.
* koncentrationer er ens: Reaktant- og produktkoncentrationer kan være forskellige, men de forbliver konstante.
* systemet er "låst": Ligevægt er en dynamisk stat. Påføring af stress (som ændring af temperatur eller tryk) vil skifte ligevægtsposition for at lindre stresset.
eksempel
Forestil dig en reversibel reaktion:
* a + b ⇌ c + d
Ved ligevægt:
* Hastigheden for A + B → C + D er lig med hastigheden på C + D → A + B.
* Koncentrationerne af A, B, C og D forbliver konstante.
* Reaktionen sker stadig, men nettoændringen i koncentrationer er nul.
Vigtige punkter
* ligevægt påvirkes af forhold: Ændringer i temperatur, tryk eller koncentration kan flytte ligevægtspositionen til at favorisere enten den forreste eller omvendte reaktion.
* ligevægtskonstant (K): Denne værdi beskriver de relative mængder af reaktanter og produkter i ligevægt. En højere k betyder, at produkterne foretrækkes i ligevægt.
Fortæl mig, hvis du har andre spørgsmål om kemisk ligevægt!
 Varme artikler
Varme artikler
-
 Mini-centrifuge til enklere undersøgelse af blodceller åbner nye organ-på-chip-mulighederFlydende metal dråbe, bruges til at lave mini-centrifugen, sidder på kanalen, hvor prøver til sidst vil blive pumpet igennem. Kredit:RMIT University En simpel innovation på størrelse med et sandko
Mini-centrifuge til enklere undersøgelse af blodceller åbner nye organ-på-chip-mulighederFlydende metal dråbe, bruges til at lave mini-centrifugen, sidder på kanalen, hvor prøver til sidst vil blive pumpet igennem. Kredit:RMIT University En simpel innovation på størrelse med et sandko -
 Forskere udvikler en optisk fiber fremstillet af gel afledt af havalgerSpiselig, biokompatibel og bionedbrydeligt, disse fibre har potentiale til forskellige medicinske anvendelser. Kredit:Eric Fujiwara En optisk fiber fremstillet af agar er blevet produceret ved Uni
Forskere udvikler en optisk fiber fremstillet af gel afledt af havalgerSpiselig, biokompatibel og bionedbrydeligt, disse fibre har potentiale til forskellige medicinske anvendelser. Kredit:Eric Fujiwara En optisk fiber fremstillet af agar er blevet produceret ved Uni -
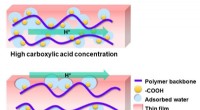 Protoners rejsevej i polymerer kan føre til rene brændstofferSkematisk repræsentation af afhængigheden af hovedprotontransportvejen i tynde polymerfilm af carboxylsyregruppekoncentrationen. Kredit:Yuki Nagao Protoner - subatomære partikler med en positiv
Protoners rejsevej i polymerer kan føre til rene brændstofferSkematisk repræsentation af afhængigheden af hovedprotontransportvejen i tynde polymerfilm af carboxylsyregruppekoncentrationen. Kredit:Yuki Nagao Protoner - subatomære partikler med en positiv -
 Ny syntesestrategi fremskynder identifikation af enklere versioner af et naturproduktBaylor University professor og kemiker Daniel Romo, Ph.D., diskuterer forskning med ph.d.-kandidat Christian M. Chaheine, medforfatter på ny syntesestrategi. Undersøgelsen er publiceret i Naturkemi
Ny syntesestrategi fremskynder identifikation af enklere versioner af et naturproduktBaylor University professor og kemiker Daniel Romo, Ph.D., diskuterer forskning med ph.d.-kandidat Christian M. Chaheine, medforfatter på ny syntesestrategi. Undersøgelsen er publiceret i Naturkemi
- Hvilken proces opstår, når vanddamp bliver til en gas kaldet og stiger luften?
- Metal midt i reaktive serier-eller et virvar?
- Hvorfor bruger folk biomasse?
- Overførsel af energi fra solen til overflade?
- Sådan beregnes metan nummer
- Ny undersøgelse viser, hvordan metan bryder gennem iskolde barrierer på havbunden


