Hvordan skelner du mellem gasserne H2 og NO2?
1. Udseende og lugt:
* H2 (brint): Farveløs, lugtfri gas.
* NO2 (nitrogendioxid): Brunlig-rød, skarp og irriterende gas med en skarp, kvælende lugt.
2. Densitet:
* H2 (brint): Den letteste gas, meget mindre tæt end luft.
* NO2 (nitrogendioxid): Tættere end luft.
3. Reaktivitet:
* H2 (brint): Meget brandfarlig og eksplosiv i nærvær af ilt.
* NO2 (nitrogendioxid): Giftig og ætsende gas, der er i stand til at reagere med vand til dannelse af salpetersyre.
4. Kemiske tests:
* H2 (brint): Forbrænder med en lyseblå flamme i luften. Kan påvises ved dens reaktion med kobberoxid til at producere vand og kobbermetal.
* NO2 (nitrogendioxid): Kan påvises ved dens reaktion med vand til at producere salpetersyre, som kan identificeres ved hjælp af lakmuspapir.
5. Spektroskopisk analyse:
* H2 (brint): Har en karakteristisk spektral signatur i de ultraviolette og infrarøde regioner.
* NO2 (nitrogendioxid): Har også en tydelig spektral signatur, især i de synlige og infrarøde regioner.
Kortfattet:
Den mest ligetil måde at skelne mellem H2 og NO2 er ved deres udseende og lugt . For mere endelig identifikation kan du dog bruge kemiske tests og spektroskopisk analyse . Husk at altid håndtere disse gasser med ekstrem forsigtighed på grund af deres potentielle farer.
Sidste artikelHvorfor er dihydrogen monosulfid polar?
Næste artikelHvad er den standard atomnotation af ilt?
 Varme artikler
Varme artikler
-
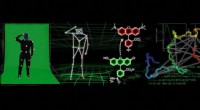 Kemikere udvikler motion capture-lignende teknologi til sporing af proteinformKredit:University of Pennsylvania I mange moderne animationsfilm, tricket til at opnå realistiske bevægelser for individuelle karakterer og objekter ligger i motion-capture teknologi. Denne proces
Kemikere udvikler motion capture-lignende teknologi til sporing af proteinformKredit:University of Pennsylvania I mange moderne animationsfilm, tricket til at opnå realistiske bevægelser for individuelle karakterer og objekter ligger i motion-capture teknologi. Denne proces -
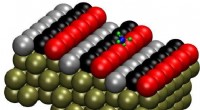 Lokalisering af den præcise reaktionsvej:Metan-dissociation på platinPt(211)-overfladen har tre-atom-brede terrasser og et-atom-høje trin. Forskerne mærkede rækken af atomer på trinkanten som trin (rød), den midterste række som terrasse (sort) og den sidste række som
Lokalisering af den præcise reaktionsvej:Metan-dissociation på platinPt(211)-overfladen har tre-atom-brede terrasser og et-atom-høje trin. Forskerne mærkede rækken af atomer på trinkanten som trin (rød), den midterste række som terrasse (sort) og den sidste række som -
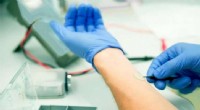 Blødt materiale inspireret af græshopper til bedre elektrodeklæbemiddelETH -forskere har udviklet en klæbende elektrode til sundhedsovervågning. En ny spin-off planlægger at bringe den på markedet i år. Kredit:ETH Zürich Forskere ved ETH Zürich har udviklet en ny typ
Blødt materiale inspireret af græshopper til bedre elektrodeklæbemiddelETH -forskere har udviklet en klæbende elektrode til sundhedsovervågning. En ny spin-off planlægger at bringe den på markedet i år. Kredit:ETH Zürich Forskere ved ETH Zürich har udviklet en ny typ -
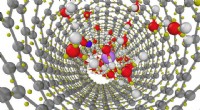 Indkredsning af virkningerne af nanoindeslutning på vandStruktur af en lithiumchloridopløsning indespærret i et 1,1 nanometer diameter carbon nanorør som opnået fra første principper molekylær dynamik simuleringer. Billede af Viktor Rozsa/University of Chi
Indkredsning af virkningerne af nanoindeslutning på vandStruktur af en lithiumchloridopløsning indespærret i et 1,1 nanometer diameter carbon nanorør som opnået fra første principper molekylær dynamik simuleringer. Billede af Viktor Rozsa/University of Chi
- Nyt værktøj registrerer samtidig magnetiske felter i forskellige retninger
- I hvilket lag af atmosfæren er Aurora Borealis?
- Induktans baseret på en kvanteeffekt har potentialet til at miniaturisere induktorer
- Materialeforskere udvikler topologisk isolator med en switch
- Hvad er materialet bevæget af erosion?
- Bryde bælgfrugter afgrøder vild relativ barriere


