Hvorfor er dihydrogen monosulfid polar?
* molekylær geometri: H₂S har en bøjet molekylær geometri, svarende til vand (H₂O). Dette skyldes de to ensomme par elektroner på svovlatomet.
* Elektronegativitet: Svovl er mere elektronegativ end brint. Dette betyder, at svovl tiltrækker de delte elektroner i H-S-bindingerne stærkere.
* annullering af dipolmomenter: Mens hver H-S-binding har et let dipolmoment, betyder den bøjede geometri, at disse dipoler annullerer hinanden. Molekylet som helhed har et nul netto dipolmoment .
Derfor er dihydrogenmonosulfid (H₂S) et ikke -polært molekyle.
Sidste artikelEr hydrogenperoxid en blanding eller rent stof?
Næste artikelHvordan skelner du mellem gasserne H2 og NO2?
 Varme artikler
Varme artikler
-
 Ikke sikker på, om du allerede har haft coronavirus? Denne test kan (måske) fortælle digMange mennesker spekulerer på, om den slemme forkølelse, de havde tilbage i februar eller marts, faktisk var den nye coronavirus. I princippet, en antistoftest kan fortælle dig, at men de fleste af te
Ikke sikker på, om du allerede har haft coronavirus? Denne test kan (måske) fortælle digMange mennesker spekulerer på, om den slemme forkølelse, de havde tilbage i februar eller marts, faktisk var den nye coronavirus. I princippet, en antistoftest kan fortælle dig, at men de fleste af te -
 Ny forskning forklarer, hvorfor nogle molekyler har uregelmæssige formerKredit:Vanderbilt University Der er altid en grund til, hvordan molekyler dannes, og hvordan de er formet. Når først forskere forstår bindingerne i molekyler, de finder ud af måder at bruge de mat
Ny forskning forklarer, hvorfor nogle molekyler har uregelmæssige formerKredit:Vanderbilt University Der er altid en grund til, hvordan molekyler dannes, og hvordan de er formet. Når først forskere forstår bindingerne i molekyler, de finder ud af måder at bruge de mat -
 En første af sin slags katalysator efterligner naturlige processer til at nedbryde plast og produce…Kredit:Unsplash/CC0 Public Domain Mens genbrug af plast ikke er ny videnskab, nuværende processer gør det ikke økonomisk umagen værd - plastaffald bliver down-cycled til lavere kvalitet, mindre br
En første af sin slags katalysator efterligner naturlige processer til at nedbryde plast og produce…Kredit:Unsplash/CC0 Public Domain Mens genbrug af plast ikke er ny videnskab, nuværende processer gør det ikke økonomisk umagen værd - plastaffald bliver down-cycled til lavere kvalitet, mindre br -
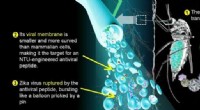 Peptid udnytter akilleshælen fra Zika-virusIllustration af forskningsresultatet. Kredit:NTU Singapore Forskere ved Nanyang Technological University, Singapore (NTU Singapore) har udviklet et antiviralt peptid, der udnytter Zika-virussen ve
Peptid udnytter akilleshælen fra Zika-virusIllustration af forskningsresultatet. Kredit:NTU Singapore Forskere ved Nanyang Technological University, Singapore (NTU Singapore) har udviklet et antiviralt peptid, der udnytter Zika-virussen ve
- To hedengangne satellitter savner snævert kollision:embedsmænd (Opdatering)
- Hvad er de to organsystemer, der er mest involveret i produktion af fysiologiske ændringer, der fø…
- Ny undersøgelse hjælper med at forklare, hvordan affaldspletter dannes i verdenshavene
- Hvorfor betragtes evolution som en videnskabelig teori?
- Hvad er forskellen mellem ophidset hydrogenatom og noget andet atom?
- Sådan beregnes pH-effekten af fortynding


