Hvorfor accepterer klor let en anden elektron?
* Elektronegativitet: Klor har en høj elektronegativitet, hvilket betyder, at det har en stærk attraktion for elektroner. Dette skyldes dets lille atomradius og det stærke træk af dens positivt ladede kerne på de ydre skalelektroner.
* ydre skal: Klor har 7 elektroner i sin yderste skal. For at opnå en stabil elektronkonfiguration skal den få en mere elektron for at afslutte sin oktet (8 elektroner i det ydre skal). Denne stabile konfiguration er som for de ædle gasser, der er kendt for deres inertitet.
Ved at få en elektron opfylder klor octetreglen derfor og når en mere stabil, lavere energitilstand. Dette er grunden til, at klor let accepterer et elektron, hvilket gør det til et meget reaktivt element.
 Varme artikler
Varme artikler
-
 Fremkomsten af kiralitet og strukturel kompleksitet i enkeltkrystaller på det molekylære og morf…Scanning af elektronmikroskopi (SEM) billeder af yo-yo-lignende, enkeltkrystaller med et flerdomæne udseende. Hver side af jojo ligner en tusindfryd blomst. Kredit:Weizmann Institute of Science Fo
Fremkomsten af kiralitet og strukturel kompleksitet i enkeltkrystaller på det molekylære og morf…Scanning af elektronmikroskopi (SEM) billeder af yo-yo-lignende, enkeltkrystaller med et flerdomæne udseende. Hver side af jojo ligner en tusindfryd blomst. Kredit:Weizmann Institute of Science Fo -
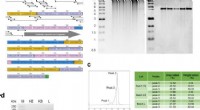 Rekombinant kollagenpolypeptid som et alsidigt knogletransplantatbiomaterialeMolekylært design og syntese af rekombinant polypeptid RCPhC1. (a) Peptidsekvensen af RCPhC1 viser Gly-Xaa-Yaa-gentagelser med aminosyresubstitutioner (rød). Alle peptidfragmenter (minimum penta-sek
Rekombinant kollagenpolypeptid som et alsidigt knogletransplantatbiomaterialeMolekylært design og syntese af rekombinant polypeptid RCPhC1. (a) Peptidsekvensen af RCPhC1 viser Gly-Xaa-Yaa-gentagelser med aminosyresubstitutioner (rød). Alle peptidfragmenter (minimum penta-sek -
 En speciel elementær magiProtoner har forskellige stabile magiske tal:2, 8, 20, 28, og så videre. Når nukleare baner er fyldt med protoner, de danner stabile kerner, analogt med ædelgaselementerne Kredit:Kyoto University/Yosh
En speciel elementær magiProtoner har forskellige stabile magiske tal:2, 8, 20, 28, og så videre. Når nukleare baner er fyldt med protoner, de danner stabile kerner, analogt med ædelgaselementerne Kredit:Kyoto University/Yosh -
 Sporing af en løsningsproces trin for trinVed hjælp af lavtemperatur scanning tunneling mikroskopi, Karsten Lucht og Karina Morgenstern kan observere individuelle molekylers adfærd i detaljer. Kredit:RUB, Marquard Kemikere fra Ruhr-Univer
Sporing af en løsningsproces trin for trinVed hjælp af lavtemperatur scanning tunneling mikroskopi, Karsten Lucht og Karina Morgenstern kan observere individuelle molekylers adfærd i detaljer. Kredit:RUB, Marquard Kemikere fra Ruhr-Univer
- Hvad er de 10 mest almindelige salte?
- Direkte observation af kohærens energiskala af Hunds metal
- Droner svæver op til skyer for at forstå effekten af isdannelse på klimaet
- Forskning kvantificerer, hvordan millioner af celler i zebrafiskembryoner påvirkes af nøglegenænd…
- Hvorfor har vi stadig offshore oliekilder? Hvordan fungerer de?
- Amazonas skovrydning har en betydelig indvirkning på det lokale klima i Brasilien


