Hvilken type oxider dannes, når metaller reagerer med ilt?
1. Grundlæggende oxider:
- dannet af stærkt reaktive metaller som alkalimetaller (gruppe 1) og alkaliske jordmetaller (gruppe 2).
- Disse oxider er ioniske og reagerer med vand for at danne metalhydroxider, som er grundlæggende.
- Eksempler:Natriumoxid (Na₂o), calciumoxid (CAO).
2. Amfoteriske oxider:
- dannet af nogle metaller som aluminium (AL) og zink (Zn).
- Disse oxider kan fungere som både syrer og baser, afhængigt af reaktionsbetingelserne.
- De reagerer med både syrer og baser for at danne salte og vand.
- Eksempler:Aluminiumoxid (al₂o₃), zinkoxid (ZnO).
Andre typer metaloxider:
- neutrale oxider: Nogle metaller som carbon (c) og nitrogen (n) danner oxider, der hverken er sure eller basale. For eksempel er carbonmonoxid (CO) et neutralt oxid.
- overgangsmetaloxider: Overgangsmetaller kan danne oxider med forskellige oxidationstilstande, hvilket fører til en lang række kemiske egenskaber.
Den dannede oxid type afhænger af metalens reaktivitet og reaktionsbetingelserne.
Sidste artikelHvad er formlen for Mercury III -oxid?
Næste artikelHvilke bindinger har calcium og klor til fælles med brintnitrogen?
 Varme artikler
Varme artikler
-
 Elbiler:Særlige farvestoffer kan forhindre unødvendige motorudskiftningerFarvestoffet tilsat harpikssystemet ændrer farve, når en alkohol, der frigives af harpiksen, binder sig til det. Kredit:Uni Halle/Alexander Funtan En dag i den nærmeste fremtid kan farvestoffer i
Elbiler:Særlige farvestoffer kan forhindre unødvendige motorudskiftningerFarvestoffet tilsat harpikssystemet ændrer farve, når en alkohol, der frigives af harpiksen, binder sig til det. Kredit:Uni Halle/Alexander Funtan En dag i den nærmeste fremtid kan farvestoffer i -
 Ionledende polymer er afgørende for at forbedre neuromorfe enhederFotografi af en neuromorf enhed brugt i denne undersøgelse. Kredit:Shunsuke Yamamoto Neuromorf refererer til efterligning af adfærden hos hjernens neurale celler. Når man taler om neuromorfe compu
Ionledende polymer er afgørende for at forbedre neuromorfe enhederFotografi af en neuromorf enhed brugt i denne undersøgelse. Kredit:Shunsuke Yamamoto Neuromorf refererer til efterligning af adfærden hos hjernens neurale celler. Når man taler om neuromorfe compu -
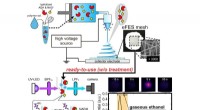 Bygning af bedre gasfasebiosensorer til bekæmpelse af sygdommeElektrospinningsenzymstrengen blev lavet med enzym- og coenzymholdig vandopløselig polymeropløsning (øverst). Det fremstillede elektrospinningsfluorometriske enzymstreng (eFES) mesh blev sat på fluore
Bygning af bedre gasfasebiosensorer til bekæmpelse af sygdommeElektrospinningsenzymstrengen blev lavet med enzym- og coenzymholdig vandopløselig polymeropløsning (øverst). Det fremstillede elektrospinningsfluorometriske enzymstreng (eFES) mesh blev sat på fluore -
 Forståelse af coronavirus-varianterKredit:Pixabay/CC0 Public Domain Med fremkomsten af nye SARS-CoV-2 varianter såsom beta og delta, folk får ikke kun et genopfriskningskursus om det græske alfabet, men også oplever forvirring og
Forståelse af coronavirus-varianterKredit:Pixabay/CC0 Public Domain Med fremkomsten af nye SARS-CoV-2 varianter såsom beta og delta, folk får ikke kun et genopfriskningskursus om det græske alfabet, men også oplever forvirring og


