Hvad er ammoniumsulfid?
Her er en sammenbrud af dens egenskaber og anvendelser:
egenskaber:
* Kemisk formel: (NH₄) ₂S
* molmasse: 68,14 g/mol
* udseende: Farveløst fast stof
* lugt: Stærk, skarp lugt af ammoniak og hydrogensulfid
* opløselighed: Meget opløselig i vand
* stabilitet: Nedbrydes i luft og lys, frigiver ammoniak og hydrogensulfidgas
* reaktivitet: Meget reaktiv, især med syrer og oxidationsmidler
anvendelser:
* Analytisk kemi: Brugt som reagens i analytisk kemi til at udfælde metalsulfider, der hjælper med identifikation og adskillelse af metaller.
* Tekstilindustri: Brugt i farvnings- og udskrivningsprocesser som et reduktionsmiddel.
* Læder garvning: Brugt i garvningsprocessen til at fjerne hår og til at blødgøre læderet.
* fungicid: Bruges som et fungicid i landbruget.
sikkerhed:
* giftig: Ammoniumsulfid er meget giftigt og bør håndteres med forsigtighed.
* irriterende: Det er en hud- og luftvejsirritant.
* brandfarlig: Det kan frigive brandfarlige gasser ved kontakt med syrer.
* opbevaring: Det skal opbevares i en tæt forseglet beholder i et køligt, tørt, godt ventileret område væk fra varme- og oxidationsmidler.
Forberedelse:
Ammoniumsulfid fremstilles typisk ved at reagere ammoniakgas med hydrogensulfidgas.
Bemærk: På grund af dets ustabilitet er ammoniumsulfid generelt ikke kommercielt tilgængelig som en ren forbindelse. Det bruges ofte som en opløsning i vand, kendt som ammoniumsulfidopløsning.
Sidste artikelHvad er den ioniske formel for gallium og svovl?
Næste artikelHvordan reagerer fluor med vand?
 Varme artikler
Varme artikler
-
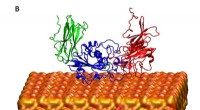 XSEDE-supercomputertildelinger på Stampede1 og Comet hjælper med at prøve proteinfoldning i knogl…XSEDE-supercomputere Stampede ved TACC og Comet ved SDSC hjalp studieforfattere med at simulere hovedstykkedomænet af cellemembranproteinreceptorintegrinet i opløsning, baseret på molekylær dynamik mo
XSEDE-supercomputertildelinger på Stampede1 og Comet hjælper med at prøve proteinfoldning i knogl…XSEDE-supercomputere Stampede ved TACC og Comet ved SDSC hjalp studieforfattere med at simulere hovedstykkedomænet af cellemembranproteinreceptorintegrinet i opløsning, baseret på molekylær dynamik mo -
 Boblefangst overflade hjælper med at slippe af med skumI to identiske bægerglas med en konstant strøm af bobler, ved at indsætte et stykke af det nye teksturerede materiale, der er udviklet af MIT -teamet (til højre), får skumdannelsen i toppen af bæger
Boblefangst overflade hjælper med at slippe af med skumI to identiske bægerglas med en konstant strøm af bobler, ved at indsætte et stykke af det nye teksturerede materiale, der er udviklet af MIT -teamet (til højre), får skumdannelsen i toppen af bæger -
 Innovationens søde smagKredit:CC0 Public Domain Ville den iskolde flaske sodavand smage så forfriskende, vel vidende at den indeholder 65 gram (5 spsk) tilsat sukker? Med en ny amerikansk fødevaremærkningspolitik sat i
Innovationens søde smagKredit:CC0 Public Domain Ville den iskolde flaske sodavand smage så forfriskende, vel vidende at den indeholder 65 gram (5 spsk) tilsat sukker? Med en ny amerikansk fødevaremærkningspolitik sat i -
 Forskere afslører mysteriet om, hvordan stråling svækker metal, ét atom ad gangenDet analyserede GB og dets omgivende miljø. (A) Automatiseret krystalorienteringskortlægning, der viser kornorienteringerne i nærheden af grænsefladen af interesse. Grænsen af interesse adskille
Forskere afslører mysteriet om, hvordan stråling svækker metal, ét atom ad gangenDet analyserede GB og dets omgivende miljø. (A) Automatiseret krystalorienteringskortlægning, der viser kornorienteringerne i nærheden af grænsefladen af interesse. Grænsen af interesse adskille
- Regeringen udgav en ny klimaændringsrapport og (Spoiler Alert) Its Really Bad
- Vildmarken i en Lake Ontario-bugt afslører, hvordan kysthabitater lider under skiftende klima, menn…
- 3-D-printet mad kan ændre, hvordan vi spiser
- Nyt materiale kan være svaret på infrastrukturproblemer
- Volkswagen og Mercedes tegner EV-batteri i overensstemmelse med Canada
- Hvad menes med et energioverførselssystem?


