Hvilken proces finder sted, når et stof kombineres med ilt?
* Gevinst af ilt: I den enkleste definition er oxidation processen, hvor et stof får iltatomer. Dette ledsages ofte af tabet af elektroner.
* Tab af elektroner: Mere generelt defineres oxidation som tab af elektroner. Dette involverer ikke nødvendigvis ilt, men ilt er en almindelig oxidation.
* Ændring i oxidationstilstand: Oxidation kan også defineres som en stigning i oxidationstilstanden for et atom eller molekyle. Oxidationstilstand er et mål for graden af oxidation af et atom i en kemisk forbindelse.
Her er nogle eksempler på oxidationsprocesser:
* Rusting: Jern reagerer med ilt i nærvær af vand til dannelse af jernoxid, almindeligt kendt som rust. Dette er et klassisk eksempel på oxidation.
* forbrænding: Brændende brændstoffer som træ, gas eller olie involverer hurtige oxidationsreaktioner, der frigiver energi i form af varme og lys.
* respiration: Levende organismer bruger ilt til at nedbryde fødevaremolekyler og frigiver energi gennem oxidationsreaktioner.
* Korrosion: Metaller, der reagerer med ilt og andre stoffer i miljøet, kan føre til deres forringelse.
Vigtig note: Det modsatte af oxidation er reduktion , hvor et stof får elektroner eller mister ilt. Disse to processer forekommer altid sammen i en kemisk reaktion kendt som en redox -reaktion .
Fortæl mig, hvis du gerne vil have en mere detaljeret forklaring af enhver specifik type oxidationsreaktion!
 Varme artikler
Varme artikler
-
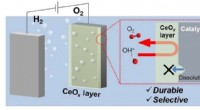 Afskærmning af iltproduktion for at holde brint på vejDen porøse belægning øger holdbarheden af oxygendannende katalysatorer, som industrien ivrigt efterspørger. Kredit:KAUST En porøs ceriumbaseret belægning øger holdbarheden af oxygendannende ka
Afskærmning af iltproduktion for at holde brint på vejDen porøse belægning øger holdbarheden af oxygendannende katalysatorer, som industrien ivrigt efterspørger. Kredit:KAUST En porøs ceriumbaseret belægning øger holdbarheden af oxygendannende ka -
 Økologisk strømlagringsbatteri lavet af vanillinTU Graz-forsker Stefan Spirk har fundet en måde at erstatte flydende elektrolytter i redoxflow-batterier med vanillin. Kredit:Lunghammer - TU Graz Forskere ved TU Graz har fundet en måde at omdann
Økologisk strømlagringsbatteri lavet af vanillinTU Graz-forsker Stefan Spirk har fundet en måde at erstatte flydende elektrolytter i redoxflow-batterier med vanillin. Kredit:Lunghammer - TU Graz Forskere ved TU Graz har fundet en måde at omdann -
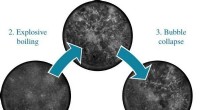 Køler rødglødende stål med varmt vandHøjhastighedsbilleder af køleprocessen. Kredit:Camila Gomez Ph.D. studerende Camila Gomez efterlignede afkølingsprocessen af Tata Steels højovne i laboratoriet og fandt ud af, at det er bedre at
Køler rødglødende stål med varmt vandHøjhastighedsbilleder af køleprocessen. Kredit:Camila Gomez Ph.D. studerende Camila Gomez efterlignede afkølingsprocessen af Tata Steels højovne i laboratoriet og fandt ud af, at det er bedre at -
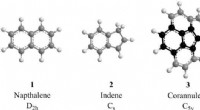 Interstellar kemi:lavtemperaturgasfasedannelse af inden i det interstellare mediumDe enkleste repræsentanter for to-ring PAHer, der bærer to seks-leddede (naphthalen, C10H8; 1) og en seks- sammen med en fem-leddet ring (indene, C9H8; 2). Mens hydrogenabstraktion-vinylacetylen-addit
Interstellar kemi:lavtemperaturgasfasedannelse af inden i det interstellare mediumDe enkleste repræsentanter for to-ring PAHer, der bærer to seks-leddede (naphthalen, C10H8; 1) og en seks- sammen med en fem-leddet ring (indene, C9H8; 2). Mens hydrogenabstraktion-vinylacetylen-addit
- Hvilket udtryk betyder under påvirkning af solen?
- Hvad er de to bevægelser, som Jorden foretager?
- Hvorfor bruge isobutan i deodorant?
- Forskning afslører oprindelsen til middelalderens altertavler
- Reflekterende lys fra satellit understøtter Wheelers kvanteteoretiske tankeeksperiment
- Fordele og ulemper ved infrarøde detektorer


