Hvad er den kemiske ligning for den reaktion af kobbersulfat, når den opvarmes?
1. Dehydrering af kobbersulfatpentahydrat:
Hvis du opvarmer kobbersulfatpentahydrat (cuso₄ · 5H₂o) , et blåt krystallinsk fast stof, vil du køre vandmolekylerne af og efterlade vandfri kobbersulfat (cuso₄), et hvidt pulver:
CUSO₄ · 5H₂O (S) → CUSO₄ (S) + 5H₂O (G)
2. Nedbrydning af vandfri kobbersulfat:
Hvis du opvarmer vandfri kobbersulfat (cuso₄) Til en meget højere temperatur nedbrydes det til kobber (II) oxid (CuO) og svovltrioxid (SO₃):
2cuso₄ (s) → 2Cuo (S) + 2SO₃ (G)
Vigtig note: Nedbrydningen af vandfri kobbersulfat forekommer typisk ved temperaturer over 650 ° C, og reaktionen er reversibel.
Fortæl mig, hvis du har andre spørgsmål om dette!
Sidste artikelHvorfor et oxid har -2 ladning?
Næste artikelEr kalium mere reaktiv eller mindre end brint?
 Varme artikler
Varme artikler
-
 Forskere designer transistorer baseret på ionisk gel lavet af en ledende polymerKredit:Pixabay/CC0 Public Domain Forskere ved University of Tsukuba har skabt en ny kulstofbaseret elektrisk enhed, π-ion gel transistorer (PIGTer) ved at bruge en ionisk gel lavet af en ledende p
Forskere designer transistorer baseret på ionisk gel lavet af en ledende polymerKredit:Pixabay/CC0 Public Domain Forskere ved University of Tsukuba har skabt en ny kulstofbaseret elektrisk enhed, π-ion gel transistorer (PIGTer) ved at bruge en ionisk gel lavet af en ledende p -
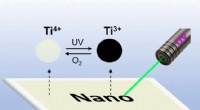 Skriv med lys på titaniumdioxid:Overskrivbare UV-følsomme overflader lavet af dopede TiO2 nanokrys…Grafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202203700 Det er lykkedes for forskere at fremstille et belægningsmateriale, der kan skrives på ved hjælp a
Skriv med lys på titaniumdioxid:Overskrivbare UV-følsomme overflader lavet af dopede TiO2 nanokrys…Grafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202203700 Det er lykkedes for forskere at fremstille et belægningsmateriale, der kan skrives på ved hjælp a -
 Økolim kan erstatte skadelige klæbemidler i træbyggeriKredit:Aalto Universitet Forskere ved Aalto Universitetet har udviklet en biobaseret klæbemiddel, der kan erstatte formaldehydholdige klæbemidler i træbyggeri. Det vigtigste råmateriale i den nye l
Økolim kan erstatte skadelige klæbemidler i træbyggeriKredit:Aalto Universitet Forskere ved Aalto Universitetet har udviklet en biobaseret klæbemiddel, der kan erstatte formaldehydholdige klæbemidler i træbyggeri. Det vigtigste råmateriale i den nye l -
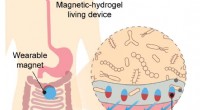 Levende sensorer undersøger tarmens mysterierSkematisk illustration af brugen af levende sensorer indkapslet i en magnetisk hydrogelanordning til undersøgelser af tarmen. Kredit:Xinyue Liu et al Forskning i den menneskelige tarm og mikrobe
Levende sensorer undersøger tarmens mysterierSkematisk illustration af brugen af levende sensorer indkapslet i en magnetisk hydrogelanordning til undersøgelser af tarmen. Kredit:Xinyue Liu et al Forskning i den menneskelige tarm og mikrobe
- Hvordan bruges observationen af forskere?
- ______ er i hvilken grad vand rent, og om det er egnet til at drikke og få planter til at vokse?
- Hvad er 238855 miles i videnskabelig notation?
- Hvilket er mindre tæt strontium eller lithium?
- Lykkeflash:Astronomer finder kosmisk radioburstkilde
- Matematiske algoritmer til grundskoleelever


