Hvad er det teoretiske udbytte af beryllium, der er nødvendig for at producere 36,0 g hydrogen?
1. Afbalanceret kemisk ligning:
Reaktionen mellem beryllium og saltsyre (HCI) producerer berylliumchlorid (BECL₂) og brintgas (H₂):
Være + 2HCl → becl₂ + h₂
2. Molforhold:
Fra den afbalancerede ligning ser vi, at 1 mol beryllium (BE) reagerer for at producere 1 mol brint (H₂).
3. Konverter masse brint til mol:
* Molmasse af H₂ =2,016 g/mol
* Mol H₂ =36,0 g / 2,016 g / mol =17,86 mol
4. Beregn mol af beryllium:
Da molforholdet for at være H₂ er 1:1, har vi brug for 17,86 mol beryllium.
5. Konverter mol af beryllium til masse:
* Molmasse af Be =9,012 g/mol
* Masse BE =17,86 mol * 9,012 g/mol = 160,9 g
Derfor er det teoretiske udbytte af beryllium, der er nødvendigt for at producere 36,0 g brint, 160,9 g.
 Varme artikler
Varme artikler
-
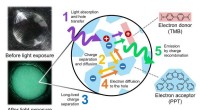 Verdens første demonstration af vedvarende luminescens fra organiske materialer, der skal låse op …En cirkulær film af glød-i-mørke organiske materialer vises i svagt omgivende lys (øverst) og i mørke efter eksponering for ultraviolet lys (nederst). Ultraviolet lys blev brugt til hurtigt at akkumul
Verdens første demonstration af vedvarende luminescens fra organiske materialer, der skal låse op …En cirkulær film af glød-i-mørke organiske materialer vises i svagt omgivende lys (øverst) og i mørke efter eksponering for ultraviolet lys (nederst). Ultraviolet lys blev brugt til hurtigt at akkumul -
 Ny analyse finder en ny mekanisme bag ældning af røde blodlegemerKredit:CC0 Public Domain Røde blodlegemer er den hyppigst forekommende celletype i blodet, transporterer ilt gennem hele menneskekroppen. I blodcirkulationen, de støder gentagne gange på forskelli
Ny analyse finder en ny mekanisme bag ældning af røde blodlegemerKredit:CC0 Public Domain Røde blodlegemer er den hyppigst forekommende celletype i blodet, transporterer ilt gennem hele menneskekroppen. I blodcirkulationen, de støder gentagne gange på forskelli -
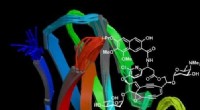 Forskere er verdens første til at reproducere en komplet kopi af anti-tumor-antibiotikumBillede der viser kromoproteinet på Kedarcidin, et komplekst anti-tumor-antibiotikum, som forskerne har reproduceret syntetisk i laboratoriet for første gang. Kredit:Professor Martin Lear, University
Forskere er verdens første til at reproducere en komplet kopi af anti-tumor-antibiotikumBillede der viser kromoproteinet på Kedarcidin, et komplekst anti-tumor-antibiotikum, som forskerne har reproduceret syntetisk i laboratoriet for første gang. Kredit:Professor Martin Lear, University -
 Fysikere tager stop-action-billeder af lysdrevet molekylær reaktionDenne illustration viser den lysinducerede ringåbningsreaktion på tværs af flere femtosekunder. Dette arbejde af forskere fra Kansas State University er netop blevet offentliggjort i Naturkemi . Kre
Fysikere tager stop-action-billeder af lysdrevet molekylær reaktionDenne illustration viser den lysinducerede ringåbningsreaktion på tværs af flere femtosekunder. Dette arbejde af forskere fra Kansas State University er netop blevet offentliggjort i Naturkemi . Kre
- Disse Android-telefoner har sikkerhedsfejl ud af æsken, siger forskere
- Fyld op! Et kig på, hvor mange penge bilejere sparer
- Robotiske superlemmer kan hjælpe månevandrere med at komme sig efter fald
- Cyberangreb på Tennessee valghjemmeside gik forud for afbrydelsen
- Antarktis effekt på havniveaustigning i de kommende århundreder
- Race og køn stadig et problem på akademiske konferencer


